
【题目】(1) 在含Fe3+的S2O![]() 和I-的混合溶液中,反应S2O
和I-的混合溶液中,反应S2O![]() (aq) + 2I-(aq)=2SO
(aq) + 2I-(aq)=2SO![]() (aq) + I2(aq)的分解机理及反应进行中的能量变化如图所示。
(aq) + I2(aq)的分解机理及反应进行中的能量变化如图所示。
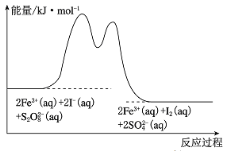
步骤①:2Fe3+(aq) + 2I-(aq) = I2(aq)+ 2Fe2+(aq)
步骤②:2Fe2+(aq) + S2O![]() (aq) = 2Fe3+(aq) + 2SO
(aq) = 2Fe3+(aq) + 2SO![]() (aq)
(aq)
下列有关该反应的说法不正确的是 _______。
A. 该反应为吸热反应
B. Fe3+是该反应的催化剂,能提高反应体系中活化分子百分数
C. 反应速率v(S2O![]() )=2v(SO
)=2v(SO![]() )
)
D. 若不加Fe3+,则正反应的活化能比逆反应的大
(2)一定条件下,工业上可采用CH3OH→CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
① 甲醇脱氢反应的第一步历程,有两种可能方式:
方式A:CH3OH*→CH3O*+H* Ea=+103.1kJ·mol-1 方式B:CH3OH*→CH3*+OH* Eb=+249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要经历的方式应为_____________。(填“A”或“B”)
②下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为 ________________________________ 。
(3)已知298K时,A、B分别为无色气体、深色气体,发生反应:A(g)![]() 2B(g)
2B(g)
①反应达平衡后,扩大容器的体积,再次达到平衡时混合气体的颜色 ____(填“变深”、“变浅”或“不变”)。
②恒容密闭容器中发生上述反应,已知v正=k正·p(A),v逆=k逆·p2(B),Kp=____________ 。(用k正、k逆表示)。若初始压强为100kPa.k正=2.8×104 s-1,当B的体积分数为40%时,v正= _____kPa·s-1[其中p(A)和p(B)分别是A和B的分压, 分压=p总×气体体积分数,k正、k逆为速率常数]
【答案】ACD A CHO*+3H*=CO*+4H* (或CHO*=CO*+H*) 变浅 ![]() 2.1×106
2.1×106
【解析】
(1) A.由图像可知反应物的总能量高于生成物的总能量,该反应为放热反应,故A错误;
B. 反应前后三价铁离子的数目性质为改变,由此可知Fe3+是该反应的催化剂,催化剂可以降低反应所需的活化能从而能提高反应体系中活化分子百分数,加快反应速率,故B正确;
C.反应速率之比等于化学计量数之比,由反应可得速率2v(S2O![]() )=v(SO
)=v(SO![]() ),故C错误;
),故C错误;
D.活化能可视为是物质到过渡态的能量,由图像可知,正反应的活化能小于逆反应的活化能,加催化剂并不能改变正逆反应活化能的相对大小,故D错误;
故答案为:ACD;
(2) 方式A所需活化能更低,所以甲醇裂解过程主要历经的方式应为A,由图象可知,相对能量从112降至65时,放出的热量最多,放热最多的步骤的化学方程式为CHO*+3H*═CO*+4H*(或CHO*═CO*+H*),故答案为:A;CHO*+3H*═CO*+4H*(或CHO*═CO*+H*);
(3) ①反应达平衡后,扩大容器的体积,各物质的浓度减小,虽然平衡正向移动,但无法抵消B浓度的下降,因此颜色变浅,故答案为:变浅;
②恒容密闭容器中发生上述反应,当反应达到平衡时v正= v逆,联立可得k正·p(A) =k逆·p2(B),Kp=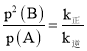 ;A(g)
;A(g)![]() 2B(g) 设起始时A的物种的量为amol,则amol气体对应的压强为100kPa,设A的变化量为xmol,列出三段式:
2B(g) 设起始时A的物种的量为amol,则amol气体对应的压强为100kPa,设A的变化量为xmol,列出三段式:

B的体积分数为40%则:![]() ,x=0.25a,此时气体的总物质的量为:1.25a,由压强之比等于气体的物质的量之比可得此时体系内压强为:125 kPa,p(A)=
,x=0.25a,此时气体的总物质的量为:1.25a,由压强之比等于气体的物质的量之比可得此时体系内压强为:125 kPa,p(A)=![]() ,v正=k正·p(A)=
,v正=k正·p(A)=![]() ,故答案为:
,故答案为:![]() ;2.1×106
;2.1×106


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】我国科技工作者设计了一种电解装置,能合成氨及硝酸,实现高效人工固氮,原理如图所示下列说法正确的是
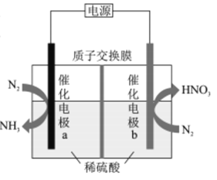
A.催化电极a的电势比催化电极b的电势高
B.负极区的电极反应为N2-10e-+6H2O=2NO3-+12H+
C.若N2得到6mole-,有6molH+向电极b迁移
D.理论上1molN2参与反应转移的电子数为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和所得结论均正确的是( )
选项 | 实验内容 | 实验结论 |
A | 向盛有5mL0.005mol/L FeCl3溶液中加入5mL0.01mol/LKSCN溶液,再继续加入少量KCl固体,观察现象 | 证明溶液存在平衡: FeCl3+3KSCNFe(SCN)3+3KCl |
B | 取两只试管,分别加入等体积等浓度的双氧水,然后试管①中加入0.01mol/LFeCl3溶液2mL,试管②中加入0.01mol/LCuCl2溶液2mL,试管①产生气泡快 | 加入FeCl3时,双氧水分解反应的活化能较大 |
C | 检验FeCl3溶液中是否含有Fe2+时,将溶液滴入酸性KMnO4溶液,溶液紫红色褪去 | 不能证明溶液中含有Fe2+ |
D | 取两只试管分别加入4mL0.01mol/LKMnO4酸性溶液,然后向一只试管中加入0.01mol/L H2C2O4溶液2mL,向另一只试管中加入0.01mol/L H2C2O4溶液4mL,第一只试管中褪色时间长 | H2C2O4浓度越大,反应速率越快 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液,反应方程式如2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56 L,计算:
(1)参加反应的HCl的物质的量________________
(2)反应中被氧化的HCl的物质的量__________________
(3)并用双线桥标出电子转移的方向和数目___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
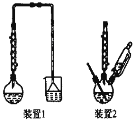
【题目】某废催化剂含SiO2、ZnO、ZnS和CuS。实验室从该废催化剂中回收锌和铜的一种流程如下图所示。
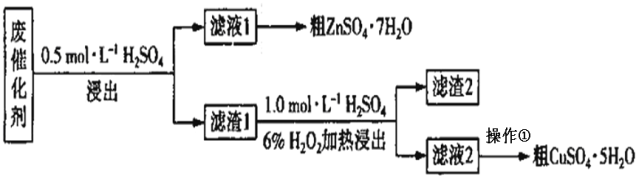
浸出使用的装置如图所示。回答下列问题:
 蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
(1)第一次浸出必须选用装置 _______(填“1”或“2”),原因是 ________。滤渣1的主要成分有_______。
(2)第二次浸出时生成单质硫,写出反应的离子方程式:_______________。该步骤即使加热温度不高也可能会有副反应发生,产物之一是空气的主要成分,分析可能原因是_____________________ 。
(3)从滤液2中得到CuSO4·5H2O的操作是 __________ 、过滤、洗涤。
(4)下列叙述中涉及到与该流程中的“操作①”相同操作的是_____________ 。
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
C.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
D. 《本草纲目》中烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”
(5)若该废催化剂中含12.8%的CuS,实验中称取15.0g废催化剂最终得到3.0gCuSO4·5H2O,则铜的回收率为 __________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用如图装置探究SO2和Fe(NO3)3溶液的反应原理。下列说法错误的是( )
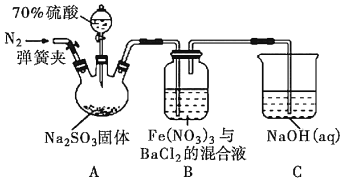
A.装置B中若产生白色沉淀,说明Fe3+能将SO2氧化成SO![]()
B.实验室中配制加70%的硫酸需要的玻璃仪器有量筒、烧杯、玻璃棒
C.三颈烧瓶中通入N2的操作应在滴加浓硫酸之前,目的是排尽装置内的空气
D.装置C可能发生倒吸,同时还不能完全吸收反应产生的尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素W、X、Y、Z的原子序数依次增加,且均不超过20。W、X、Y最外层电子数之和为15,![]() 是实验室常用的一种化学试剂。下列说法中错误的是( )
是实验室常用的一种化学试剂。下列说法中错误的是( )
A.Z2Y的水溶液呈碱性
B.最简单氢化物沸点高低为:X>W
C.常见单质的氧化性强弱为:W>Y
D.![]() 中各原子最外层均满足8电子稳定结构
中各原子最外层均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A. C生成的速率与C分解的速率相等
B. 单位时间内消耗amolA,同时生成3amolC
C. 容器内的压强不再变化
D. 混合气体的物质的量不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com