
【题目】氧化铜、氯化亚铜是重要的化工原料,广泛用作有机合成的催化剂。
Ⅰ.实验室用右图所示装置,利用还原铜粉和氯气来制备氧化铜。
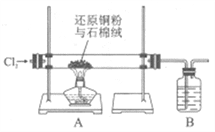
(1)石棉绒的作用是_______________。
(2)装置B中的试剂是_______________。
(3)所得产品中CuCl2的质量分数为90%,则其中可能含有的杂质是_______________(写一种即可)。
Ⅱ.另取纯净CuCl2固体用于制备CuCl。
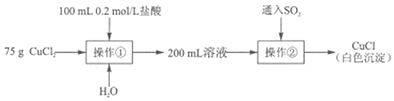
(4)操作①中加入盐酸的目的主要是_______________。
(5)操作②中反应的离子方程式为_______________。
(6)操作①中若用10mol/L盐酸代替0.2mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。
为验证此猜想,取75gCuCl2固体、100mL0.2mol/L盐酸及_______________mL9.8mol/LH2SO4配制成200mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:c(Cl-)过大导致白色沉淀溶解。
[资料显示:存在平衡2Cl-(aq)+CuCl(s)![]() CuCl32-(aq)]
CuCl32-(aq)]
请设计实验说明该猜想是否成立:________________。
【答案】 增大铜粉与氯气的接触面积 NaOH溶液 Cu或CuCl或石棉绒 Cu2++2H2O![]() Cu(OH)2+2H+ 酸抑制Cu2+的水解 2Cu2++SO2+2Cl-+2H2O=SO42-+2CuC1↓+4H+ 50 取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立。
Cu(OH)2+2H+ 酸抑制Cu2+的水解 2Cu2++SO2+2Cl-+2H2O=SO42-+2CuC1↓+4H+ 50 取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立。
【解析】(1)石棉绒的作用是增大铜粉与氯气的接触面积;正确答案:增大铜粉与氯气的接触面积。
(2) 氯气有毒, 可用氢氧化钠溶液吸收,所以B装置是吸收尾气;正确答案:NaOH溶液。 (3)根据反应前后元素守恒规律:氯气和铜反应除了生成CuCl2外,还可能有CuCl生成,还可能有铜剩余,或有石棉绒夹杂;因此可能含有的杂质是Cu或CuCl或石棉绒;正确答案:Cu或CuCl或石棉绒。
Ⅱ.(4) 因为氯化铜是强酸弱碱盐,溶液中存在Cu2++2H2O![]() Cu(OH)2+2H+ ,所以溶解时加入HCl溶液,抑制氯化铜的水解;正确答案:Cu2++2H2O
Cu(OH)2+2H+ ,所以溶解时加入HCl溶液,抑制氯化铜的水解;正确答案:Cu2++2H2O![]() Cu(OH)2+2H+ 酸抑制Cu2+的水解。
Cu(OH)2+2H+ 酸抑制Cu2+的水解。
(5) 操作②为向含有铜离子、氯离子的溶液中通入二氧化硫气体,生成CuC1沉淀,反应为2Cu2++SO2+2Cl-+2H2O=SO42-+2CuC1↓+4H+ ;正确答案:2Cu2++SO2+2Cl-+2H2O=SO42-+2CuC1↓+4H+↓。
(6)设9.8mol/LH2SO4的体积为VmL,则0.2×0.1+V×9.8×2=10×0.1, 解之得V=50mL;体系中存在平衡2Cl-(aq)+CuCl(s)![]() CuCl32-(aq),溶液中氯离子的浓度过大平衡正向移动,可以取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立;正确答案:50;取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立。
CuCl32-(aq),溶液中氯离子的浓度过大平衡正向移动,可以取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立;正确答案:50;取少量白色沉淀加入到饱和氯化钠溶液中,搅拌,若白色沉淀溶解,说明猜想二成立,反之不成立。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
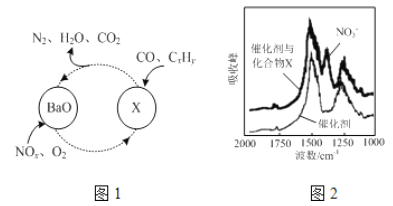
①在图示的转化中,被还原的元素是_______________,X的化学式为__________________。
②钡元素在周期表中的位置是___________________________。
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的最之比为2:1时,写出发生反应的化学方程式:____________________________。
(3)利用ClO2氧化氮氧化物反应过程如下:NO![]() NO2
NO2![]() N2反应I的化学方程式是2NO+ ClO2+H2O==NO2+HNO3+ 2HCl,反应II的离子方程式是__________________。
N2反应I的化学方程式是2NO+ ClO2+H2O==NO2+HNO3+ 2HCl,反应II的离子方程式是__________________。
(4)加入过量次氯酸钠可使废水中NH4+完全转化为N2,而本身被还原为NaCl。
①检验废水中是否存在NH4+的方法是_______________________________________________。
②若处理废水产生了0.448LN2 (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解精炼铜的说法中不正确的是
A. 电解质溶液中要含有Cu2+
B. 粗铜作阳极,精铜作阴极
C. 电解时,阳极发生氧化反应,阴极发生还原反应
D. 粗铜中所含Zn、Fe、Ni等杂质电解后以单质形式沉枳于阳极泥中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1;将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)![]() CuSO4(s) +5H2O(
CuSO4(s) +5H2O(![]() ),热效应为ΔH3。则下列判断正确的是
),热效应为ΔH3。则下列判断正确的是
A. ΔH2>ΔH3 B. ΔH1<ΔH3
C. ΔH1+ΔH3=ΔH2 D. ΔH1+ΔH2=ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生的实验报告中,描述合理的是
A. 用托盘天平称量25.20g NaCl
B. 用pH试纸测得NaClO溶液的pH约为11
C. 用25mL碱式滴定管量取出15.00mLKMnO4溶液
D. 将CuSO4溶液蒸发浓缩、降温结晶、过滤得到硫酸铜晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) H1=-1160kJ/mol
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) H2=-574kJ/mol
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体。
①该混合气体中NO和NO2的物质的量之比为________;
②在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式:________.
(2)以甲烷为燃料的新型燃料电池,其成本大大低于以氢气为燃料的传统燃料电池,目前已得到了广泛的研究。如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。
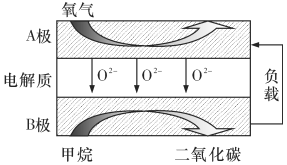
①B极为电池________极,电极反应式为________。
②若用该燃料电池作电源,用石墨作电极电解100mL1mol/L的硫酸铜溶液,写出阳极的电极反应式:_______;标准状况下,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为________,实际上消耗的甲烷体积(已折算成标准状况下)比理论上大,可能原因为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香族化合物A的分子中含有C、H、O.N四种元素,相同状况下,其蒸气的密度是氢气密度的68.5倍。现以苯为原料合成A,并最终制得F(一种染料中间体),转化关系如下图所示(一些非主要产物已略去):
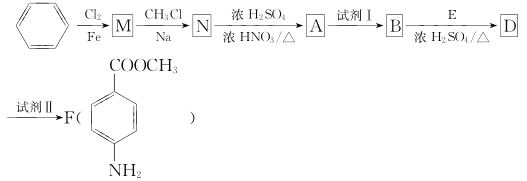
已知:
I.R-Cl+2Na+Cl-R'→R-R'+2NaCl(R、R'为烃基);
Ⅱ. 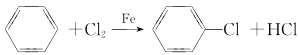
Ⅲ.  (苯胺,弱碱性,易被氧化)。
(苯胺,弱碱性,易被氧化)。
请回答下列问题:
(1)写出A的分子式:_____________。
(2)N→A的反应类型是____________。
(3)上述转化中的试剂Ⅱ是__________(填字母代号)。
a.KMnO4(H+) b.Fe/盐酸 c.NaOH溶液
(4)用核磁共振氢谱可以证明化合物E中含有______种处于不同化学环境的氢。
(5)同时符合下列两个要求的D的同分异构体有_____种。
①属于芳香族化合物,分子中只有两个互为对位的取代基,其中一个取代基是硝基;
②分子中含有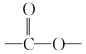 结构。
结构。
其中有一种D的同分异构体W,其在酸性条件下水解后,可得到一种能与FeCl3溶液发生显色反应的产物,写出W在酸性条件下水解的化学方程式:_________________。
(6)F在一定条件下的水解反应如下所示:
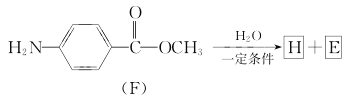
化合物H在一定条件下经缩聚反应可制得高分子纤维,该高分子纤维可广泛应用于通讯、导弹、宇航等领域。请写出该缩聚反应的化学方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]()
![]() (注:R、R′表示烃基),
(注:R、R′表示烃基),![]() 属于酮类,酮不发生银镜反应。今有如下变化:A(C6H12O2)
属于酮类,酮不发生银镜反应。今有如下变化:A(C6H12O2)![]()
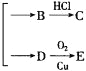 。已知C为羧酸,C、E都不发生银镜反应,则A的结构可能有
。已知C为羧酸,C、E都不发生银镜反应,则A的结构可能有
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com