
| A. | 5.6g | B. | 2.8g | C. | 11.2g | D. | 1.4g |
分析 Fe、FeO、Fe2O3的混合物中加入盐酸恰好使混合物完全溶解,生成了铁的氯化物,因加入KSCN 溶液,无血红色出现,说明只生成氯化亚铁,根据氯元素守恒可知道氯化亚铁的量,进而求得铁元素的质量.
解答 解:用盐酸溶解后,得到的产物加 KSCN 溶液,无血红色出现,说明得到的产物是氯化亚铁,即混合物中的铁元素全在氯化亚铁中,
盐酸的物质的量为1mol.L-1×0.1L=0.1mol,
根据氯元素守恒,则n(Fe)=n(FeCl2)=$\frac{1}{2}$×n(HCl)=0.05mol,
则混合物中Fe元素的质量为m(Fe)=0.05mol×56g/mol=2.8g,
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,采用原子守恒或得失电子守恒可简化计算,试题培养了学生的化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的电子式:N??N | |
| B. | 质子数为53,中子数为78的碘原子:78131I | |
| C. | S2-的结构示意图: | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3=Fe3++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
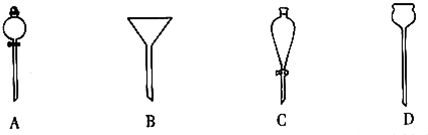
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 室内着火被困,立即用湿毛巾堵住口鼻,匍匐前进,寻找安全出口 | |
| B. | 电石燃烧时,可以用常规的水枪灭火 | |
| C. | 误服食品袋中的干燥剂(生石灰),立即喝食醋 | |
| D. | 少量的浓硫酸沾到皮肤上,立即用大量的水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl的电子式: | B. | 中子数为7的碳原子:13C | ||
| C. | Cl的原子结构示意图: | D. | 次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食用加碘食盐以防止碘缺乏病 | |
| B. | 使用铁锅炒菜可以减少贫血病的发生 | |
| C. | 保持科学的饮食习惯,全面摄入各种微量元素 | |
| D. | 多吃各种营养品,以增大微量元素的吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com