

| △n |
| V?△t |
| △n |
| V?△t |
| 0.5mol |
| 2L×5min |
| (3×10-3)2 |
| (2.5×10-1)×(4.0×1-2) |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | V | W | X | Y | Z |
| 原子半径(×0.1nm) | 0.37 | 0.77 | 0.75 | 0.74 | 1.85 |
| 电负性 | 2.1 | 2.5 | 3.0 | 3.5 | 1.66 |
| 常见化合价 | +1 | +4,-4 | +5,+3,-3 | -2 | +6,+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、只有①③⑤ |
| C、②③⑤⑥ | D、只有③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
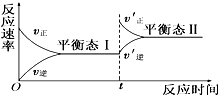 如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )
如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )| A、平衡态Ⅰ与平衡态Ⅱ的正反应速率相等 |
| B、平衡移动的原因可能是增大了反应物浓度 |
| C、平衡移动的原因可能是增大了压强 |
| D、平衡状态Ⅰ和平衡状态Ⅱ的平衡常数的大小关系为K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不变 | B、增大 |
| C、减小 | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“是药三分毒”,必须按医嘱或药物说明书使用药物,防范不良反应 |
| B、使用青霉素时,直接静脉注射,可以不用进行皮肤敏感试验 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、对于标记“OTC”的药物,必须持有医生的处方才能购买 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com