
(10分)常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
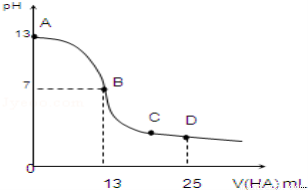
(1)写出MOH的电离方程式:__________________
(2)MOH与HA恰好完全反应时,溶液呈________性(填“酸”、“碱”或“中”),理由是(用离子方程式表示):__________;此时,混合溶液中由水电离出的c(H+)_________0.2mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(3)写出B点,混合溶液中各离子浓度的大小关系B点____________.
(4)D点时,溶液中c(A﹣)+c(HA)__________2c(M+)(填“>”、“<”或“=”).
科目:高中化学 来源:2016届江苏省淮安市高三上学期11月月考化学试卷(解析版) 题型:填空题
碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如下:

(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是 。
(2)已知Ksp[Ni(OH)2]=2×10-15,欲使NiSO4溶液中残留c(Ni2+)≤2×10-5 mol·L-1,调节pH的范围是 。
(3)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式: 。
(4)若加热不充分,制得的NiOOH中会混有Ni(OH)2,其组成可表示为xNiOOH·yNi(OH)2。现称取9.18 g样品溶于稀硫酸,加入100 mL 1.0 mol·L-1 Fe2+标准溶液,搅拌至溶液清亮,定容至200 mL。取出20.00 mL,用0.010 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定x、y的值(写出计算过程)。涉及反应如下(均未配平):
NiOOH+Fe2++H+—Ni2++Fe3++H2O Fe2++MnO4-+H+—Fe3++Mn2++H2O
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期10月阶段性教学质检化学试卷(解析版) 题型:选择题
将铁片放入下列溶液中,溶液质量增加,但没有气体放出的是
A.稀硫酸 B.CuSO4溶液 C.FeCl3溶液 D.稀硝酸
查看答案和解析>>
科目:高中化学 来源:2016届四川省德阳市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
甲乙丙是三种不含相同离子的可溶性电解质。他们所含的离子如表所示。取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)<c(乙)<c(丙),下列说法正确的是
阳离子 | Na+ NH4+ Fe3+ |
阴离子 | OH- Cl- SO42- |
A、甲中一定含有Na+ B、乙中一定含有NH4+
C、丙中一定含有 Fe3+ D、丙中一定含有SO42-
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高三上学期10月月考化学试卷(解析版) 题型:选择题
Cl2、HCl的混合气体通入足量的氢氧化钠溶液,充分反应后分析产物溶液中除大量OH? 外,还有Cl?、ClO?、ClO3?,并知这三种离子的物质的量比为9:2:1。试问原混合气体中Cl2与HCl体积比为
外,还有Cl?、ClO?、ClO3?,并知这三种离子的物质的量比为9:2:1。试问原混合气体中Cl2与HCl体积比为
A.5:2 B.3:1  C.2:5 D.1:1
C.2:5 D.1:1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中测试化学试卷(解析版) 题型:选择题
下列物质分类组合正确的是
A | B | C | D | |
强电解质 | HBr | FeCl3 | H3PO4 | Ca(OH)2 |
弱电解质 | HF | CH3COOH | BaSO4 | HI |
非电解质 | NH3 | Cu | H2O | C2H5OH |
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+ 和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
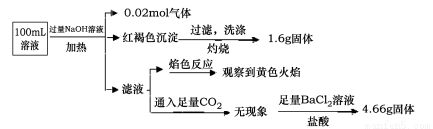
由此可知原溶液中
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol·L-1
C.SO42ˉ、NH4+ 、Na+一定存在,CO32ˉ、Al3+一定不存在
D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入足量酸性高锰酸钾溶液,若溶液紫红色褪去,则证明原溶液中有Fe2+
查看答案和解析>>
科目:高中化学 来源:2016届浙江省新安江校区高三上学期第二次模拟化学试卷(解析版) 题型:推断题
(10分)酸牛奶是人们喜爱的一种营养饮料。酸牛奶中有乳酸菌可产生乳酸等有机酸,使酸碱度降低,有效地抑制肠道内病菌的繁殖。酸牛奶中的乳酸可增进食欲,促进胃液分泌,增强肠胃的消化功能,对人体具有长寿和保健作用,乳酸的结构为:
工业上它可由乙烯来合成,方法如下:

(1)乳酸所含的官能团的名称是 .
(2)写出下列转化的化学方程式:
①A的生成 .
②C的生成 .
③乳酸在一定条件合成聚乳酸 .
(3)写出符合下列要求的乳酸的所有同分异构体的结构简式
a、属于酯类, b、含有-OH, c、能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2016届山东省邹城市高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24 L CCl4中含Cl原子数目为0.4NA
B.白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA
C.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA
D.5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com