
电解质溶液的电导率越大,导电能力越强。用0.100mol·L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液电导率如图所示。下列说法不正确的是( )
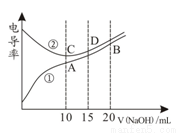
A.曲线①代表滴定CH3COOH溶液的曲线
B.在相同温度下,A、B、C 三点溶液中水电离的 c(H+):B<A=C
C.D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
D.A点溶液中:c(CH3COO-)+c(OH-)-c(H+) = 0.05mol·L-1
 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源:2016-2017学年浙江省温州市十校联合体高一上期末化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 核素23Na的中子数是12
B. 16O和18O互为同位素
C. 电离方程式:CH3COOH CH3COOˉ+H+
CH3COOˉ+H+
D. 16O、1H、2H、3H四种核素可构成4种水分子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上期末化学卷(解析版) 题型:实验题
氯气在工业上有着重要的用途,某兴趣小组在实验室中用下列装置模拟工业上用氯气制备无水氯化铝(183℃时升华,遇潮湿空气即产生大量白雾)。
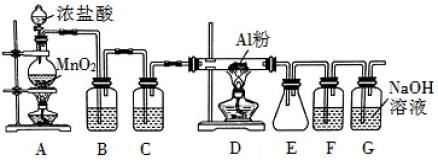
 请回答下列问题:
请回答下列问题:
(1)装置 B 中盛放饱和食盐水,其作用是 。F 中盛放的是 ,其作用是 。用一件仪器装填适当试剂后也可起到 F 和 G 的作用,所装填的试剂为 。
(2)装置 A 实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
A.往烧瓶中加入 MnO2 粉末 B.加热 C.往烧瓶中加入浓盐酸
(3)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学 提出很多实验方案,其中方案之一为让残留的液体与足量 Zn 反应,测量生成的 H2体积。 装置如图所示(夹持器具已略去)。反应完毕,每间隔 1 分钟读取气体体积、气体体积逐渐减小,直至不变。气体体积逐次减小的原因是 (排除仪器和实验操作的影响因素)。
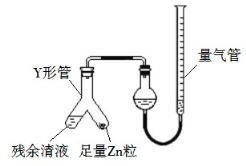
(4)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量 ClO2 生成;ClO2 沸点为 10 ℃,熔点为?59 ℃,液体为红色;Cl2 沸点为?34 ℃,液态为黄绿色。设计最简单的实验验证 Cl2中含有 ClO2: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上期末化学卷(解析版) 题型:选择题
下列有关元素及其化合物的说法正确的是
A.水蒸气通过灼热的铁粉生成氢氧化铁和氢气
B.FeCl3 既能通过化合反应制得,也能通过金属与酸的置换反应制得
C.Na 在空气中长期放置最终变为 Na2CO3 粉末
D.向 KClO3 溶液中滴加 AgNO3 溶液得到白色 AgCl 沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省等名校高二上期末化学卷(解析版) 题型:填空题
铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的 CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
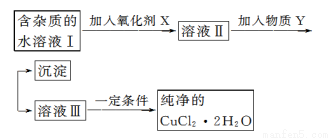
已知Cu2+、 Fe3+和 Fe2+的氢氧化物开始沉淀和沉淀完全时的 pH,见下表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的 pH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的 pH | 3.0 | 9.0 | 6.7 |
请回答下列问题:
(1)常温下,计算Fe(OH)3的溶度积Ksp=________(通常认为残留在溶液中的离子浓度小于1×10-5 mol/L 时则沉淀完全。)
(2)加入氧化剂的目的______________________。
(3)最适合作氧化剂X的是__________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(4)加入的物质 Y 是____________。
(5)若向溶液Ⅱ中加入碳酸钙,产生的现象是____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省等名校高二上期末化学卷(解析版) 题型:选择题
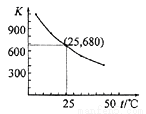
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)  I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
A.反应I2(aq)+I-(aq)  I3 -(aq)的ΔH>0
I3 -(aq)的ΔH>0
B.利用该反应可以除去硫粉中少量的碘单质
C.在上述平衡体系中加入苯,平衡不移动
D.25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省等名校高二上期末化学卷(解析版) 题型:选择题
如图装置放置一段时间后,铁钉均被腐蚀。下列有关描述不正确的是( )
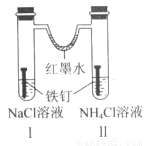
A.红墨水水柱两边的液面变为左低右高
B.I 和Ⅱ中负极反应式均为 Fe-2e-=Fe2+
C.I 中正极反应式为 O2+2H2O+4e-=4OH
D.Ⅱ中 NH4Cl 溶液里有气泡产生
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期期末化学试卷(解析版) 题型:选择题
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知
A. X的原子半径大于Y的原子半径
B. X的电负性大于Y的电负性
C. X的氧化性小于Y的氧化性
D. X的第一电离能小于Y的第一电离能
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省广安市高一上学期期末化学试卷(解析版) 题型:填空题
(1)按要求填写下列空格(设阿伏加德罗常数为NA)
①39 g Na2O2中的Na+_________ NA;
②0.5mol H2O中的质子数为_________NA;
③1.204×1024个水分子的质量为_________ g;
④标准状况下,10g CO和CO2混合气体的体积是6.72L,则此混合气体中,CO和CO2的物质的量之比是 ;
⑤9.2g氮的氧化物NOx中含有N原子数为0.2mol,则x数值为 。
(2)用于分离或提纯物质的方法有:
A蒸馏(分馏) B萃取 C过滤 D重结晶 E分液
分离或提纯下列各组混合物 ,请选择上述最合适的方法的标号填在橫线上。
,请选择上述最合适的方法的标号填在橫线上。
①除去Ca(OH)2溶液中悬浮的CaCO3微粒 ;
②分离四氯化碳与水的混合物 ;
③分离汽油和柴油 ;
④提纯氯化钠和硝酸钾混合溶液中的硝酸钾 。
(3)找出下列各组物质中与另三种物质的类别不同的一种物质,用化学式填写在后面的横线上。
① CaO、Na2O、CO2、CuO ;
② H2、N2、P、Cu ;
③ S、Fe、Cu、Zn ;
④ HCl、H2O、H2SO4、HNO3 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com