
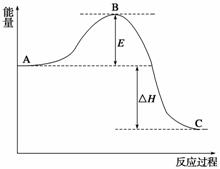
2SO2(g)+O2(g)2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
请回答下列问题:
(1)图中A、C分别表示__________、__________,E的大小对该反应的反应热有无影响?__________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________,理由是_________________________________________________________;
(2)图中ΔH=__________kJ·mol-1;
(3)V2O5的催化循环机理可能为V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:________________________________________________________________________;
(4)已知常温下,1 mol固体硫燃烧生成二氧化硫气体时放出的热量是296 kJ,计算由S(s)生成3 mol SO3(g)的ΔH________(要求写出计算过程)。
答案 (1)反应物总能量 生成物总能量 无 降低 因为催化剂改变了反应历程,使活化能E降低
(2)-198
(3)SO2+V2O5===SO3+2VO2、4VO2+O2===2V2O5
(4)S(s)+O2(g)===SO2(g) ΔH1=-296 kJ·mol-1,SO2(g)+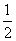 O2(g)===SO3(g) ΔH2=-99 kJ·mol-1,3S(s)+
O2(g)===SO3(g) ΔH2=-99 kJ·mol-1,3S(s)+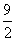 O2(g)===3SO3(g) ΔH=3(ΔH1+ΔH2)=-1 185 kJ·mol-1
O2(g)===3SO3(g) ΔH=3(ΔH1+ΔH2)=-1 185 kJ·mol-1
解析 (1)反应物总能量高于生成物总能量为放热反应 ,由图可得到A和C所表示的意义,E为活化能与反应热无关,但是使用催化剂可以降低反应活化能;
(2)图中表示的是2 mol SO2的反应,因此ΔH=-99×2 kJ·mol-1=-198 kJ·mol-1;
(3)依题意即可写出:SO2+V2O5===SO3+2VO2、4VO2+O2===2V2O5。


科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.4 4 g CO2气体中所含原子数为2 NA
B.常温常压下,22.4 L氢气所含原子数为2 NA
C.1 L mo l·L-1的硫酸钠溶液中钠离子数为2 NA
D.在Cl2参与的反应中,1 mol Cl2得到的电子数一定是2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.pH<7的溶液不一定是酸溶液
B.常温下,pH=5的溶液和pH=3的溶液相比,前者[OH-]不一定是后者的100倍
C.室温下,每1×107个水分子中只有一个水分子发生电离
D.在1 mol·L-1的氨水中,改变外界条件使[NH4+]增大,则溶液的pH一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的打“√”,错误的打“×”
(1)所有的燃烧反应都是放热反应,所以不需要加热就能进行( )
(2)反应物的总能量低于生成物的总能量时,一定不能发生反应( )
(3)物理变化过程中,也可能有热量的变化( )
(4)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
(5)一个反应的焓变因反应物的用量和反应条件的改变而发生改变( )
(6)催化剂能改变反应的焓变( )
(7)已知S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ·mol-1,则S(s)+O2(g)===SO2(g)反应放出的热量大于293.23 kJ·mol-1( )
(8)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH不同( )
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2C+O2===2CO的能量变化如图所示。下列说法正确的是( )
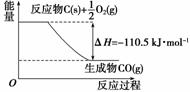
A.12 g C(s)与一定量O2(g)反应生成14 g CO(g),放出的热量为110.5 kJ
B.2 mol C(s)与足量O2(g)反应生成CO2(g),放出的热量大于221 kJ
C.该反应的热化学方程式是2C(s)+O2(g)===2CO(g)
ΔH=-221 kJ
D.该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2(g)2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1,2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束后,所剩余的固体滤出后能被磁铁吸引,反应后溶液存在较多的阳离子是 ( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Ca2+、Cl-、SO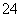
B.Fe2+、H+、SO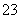 、ClO-
、ClO-
C.Mg2+、NH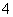 、Cl-、SO
、Cl-、SO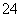
D.K+、Fe3+、NO 、SCN-
、SCN-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com