
【题目】有机物W 在工业上常用作溶剂和香料,其合成方法如下:
![]()
下列说法正确的是
A. N、W 互为同系物
B. M、N、W 均能发生加成反应和取代反应
C. W 能发生皂化反应
D. M 的二氯代物有8种
【答案】B
【解析】A、N含有官能力为羧基,属于羧酸类,W含有官能团为酯基,属于酯类,不是同系物,选项A错误;B、M、N、W 三种有机物结构中均含有苯环,均能与氢气发生加成反应,M能够与溴、铁作催化剂发生取代反应生成溴苯,N能与醇发生酯化反应,W能在酸性或碱性环境下发生水解反应,选项B正确;C、高级脂肪酸甘油酯在碱性环境下水解为皂化反应,W不属于高级脂肪酸甘油酯,能够与碱反应,但不是皂化反应,选项C错误;D、M的二氯代物有:环上有2个氯、1个甲基,这样的有机物有6种,环上有一个CHCl2,只有1种,环上有1个氯、1个CH2Cl,这样的有机物有3种,共计有10种,选项D错误。答案选B。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】下面是生物体细胞内部分有机化合物的概念图,请回答下列问题。
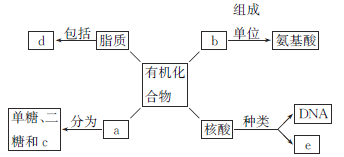
(1)小麦种子中的储能物质c是________,人和动物细胞中的储能物质c是________。
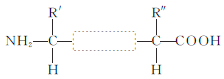
(2)两个氨基酸发生脱水缩合反应时,产物是________和________,下图方框内的结构简式是________。
(3)b结构的多样性决定其功能的多样性,如作为结构物质、防御物质、________、________、调控物质等。
(4)SARS病毒的遗传信息贮存在e中,e物质初步水解的产物是______________;在小麦叶肉细胞中,e主要存在于________中。
(5)d中构成生物膜的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成。下图是用燃烧法确定有机物化学式常用的装置,该方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。

回答下列问题:
(1)A装置中发生反应的化学方程式为______________________________________,
(2)C装置(燃烧管)中CuO的作用是_______________________________________,
(3)写出E装置中所盛放试剂的名称_____________,
(4)将4.6 g有机物M进行实验,测得生成5.4 g H2O和8.8 g CO2,则该物质的实验式是________。
(5)经测定,有机物M的核磁共振氢谱示意图如图,则M的结构简式为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。
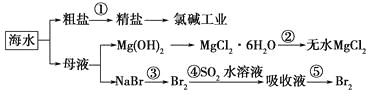
下列有关说法正确的是( )。
A. 第①步中除去粗盐中的SO42—、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液―→NaOH溶液―→BaCl2溶液―→过滤后加盐酸
B. 工业上通过氯碱工业制取金属钠
C. 从第③步到第⑤步的目的是浓缩、富集溴单质
D. 第②步的反应条件是高温加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的HA溶液,溶液的PH与所加NaOH溶液体积(V)的关系如图所示。下列说法不正确的是
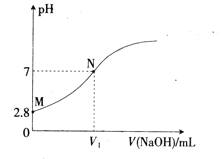
A. V1<20
B. Ka(HA)的数量级为10-5
C. M点溶液加少量水稀释,c(H+)/c(A-)增大
D. N点后,随着NaOH溶液的加入,溶液中水的电离程度逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:
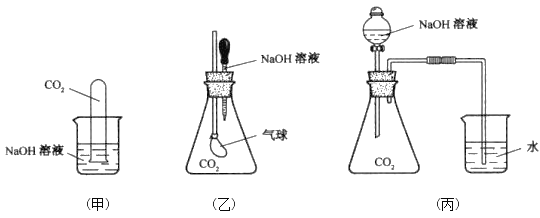
(1)请写出甲实验中CO2与过量的NaOH发生反应的离子方程式:__________。
(2)丙实验装置的实验现象是________________________。
(3)乙实验中,如果二氧化碳和氢氧化物的物质的量之比为1:1.5,且恰好完全反应,溶液中含有的溶质主要是_______________。
A、NaOH 和Na2CO3 B、Na2CO3 C、Na2CO3和NaHCO3 D、NaHCO3
Ⅱ、为探究碳酸钠和碳酸氢钠固体的热稳定性,某同学设计了“套管实验”,装置如图:
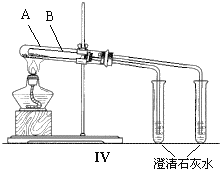
(1)小试管B中应装的药品是________(写化学式)。
(2)和大试管A相连的装有澄清石灰水的小试管中出现的现象预计是____________________。
Ⅲ、工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)称取质量为m1 g的样品溶解后加入过量的CaCl2溶液,将所得沉淀______________(填操作)、洗涤、烘干、称量得到m2 g固体,则Na2CO3的质量分数是_____________________。
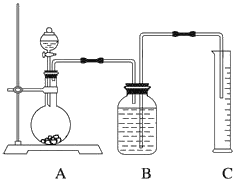
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应,用下图所示装置测定产生CO2的体积,实验结束后,量筒中得到V mL液体,则反应中生成二氧化碳的物质的量是____________(题目中气体体积均已经换算成标准状况),为了确保测定结果的准确性,B中的溶液为饱和碳酸氢钠,因为二氧化碳难溶于饱和碳酸氢钠,但选用该溶液后实验结果仍然不够准确,Na2CO3的质量分数偏大,其原因可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)①Fe原子的核外电子排布式为[Ar]_________,Mg原子核外占据最高能层电子的电子云轮廓图形状为_________。
②As的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是_________,AsCl3分子的立体构型为_________。
(2)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式为

以下关于维生素B1的说法正确的是________。
A.只含σ键和π键
B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl
D.该物质易溶于盐酸
(3)维生素B1晶体溶于水的过程中要克服的微粒间作用力有________。
A.离子键、共价键 B.离子键、氢键、共价键
C.氢键、范德华力 D.离子键、氢键、范德华力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com