
碳酸钙和硫酸钙都是钙的重要化合物,它们在生产生活中都有着广泛的应用。甲、乙两组同学分别对碳酸钙的制备、硫酸钙的性质进行了以下探究,请你参与并完成对有关问题的解答。
(1)甲组使用大理石(含少量的Fe2O3杂质)等物质制备碳酸钙的实验流程如下: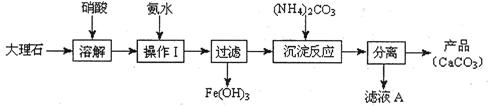
①溶解大理石时,用硝酸而不用硫酸的原因是 。
②上述流程中,“分离”得产品所包含的实验操作依次为:过滤、 、 。
③“滤液A”中除H+离子外,还含有的阳离子是 ;检验该阳离子的实验方法是:取少量滤液A与 在试管中混合、加热充分反应,将湿润的红色石蕊试纸(或pH试纸)靠近试管口,观察现象即可。
(2)乙组对某硫酸钙晶体(xCaS04·yH20)加热分解的有关反应进行探究。他们取6.52g该晶体进行加热,加热过程中,固体质量随时间的变化情况如下图所示。又知t5~t6时间段内固体质量减轻的原因是产生了两种气体,反应的化学方程式为:2CasO4 2CaO+2S02↑+O2↑。
2CaO+2S02↑+O2↑。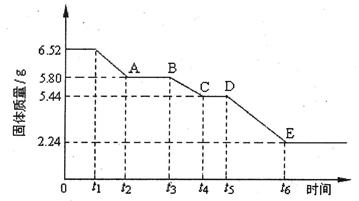
①加热时,该晶体开始发生化学变化的时间是 (填“t1”、“t3”或“t5”)。
②t4~t5时间段固体的化学式为 。
③tl~t2时间段固体发生反应的化学方程式为 。
(1)①硫酸钙微溶于水(1分)
②洗涤(1分) 干燥(1分)
③NH4+(或铵根离子)(1分) 烧碱(溶液)(1分)
(2)①t1(1分)
②CaSO4(2分)
③2CaSO4·3H2O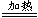 2CaSO4·H2O+2H2O(2分)
2CaSO4·H2O+2H2O(2分)
解析试题分析:(1)①大理石与硫酸反应生成微溶的硫酸钙附着在大理石表面,阻碍反应的进行;②分离操作后得到产品碳酸钙,故先过滤得到沉淀,再经过洗涤、干燥等制的纯净的样品;③滤液A是碳酸铵和硝酸钙反应后的溶液,阳离子含有铵根离子;(2)晶体的质量开始变小,就开始化学变化,先失去结晶水,后硫酸钙分解。根据图示最后反应生成氧化钙,
n(CaO)=2.24÷56=0.04mol 样品中n(H2O)=(6.52-0.04×136)÷18=0.06mol
化学式为 2CaS04·3H20
AB端产物判断n(H2O)=(6.52-5.80)÷18=0.04mol,剩余水为0.03mol
产物化学式为2CaS04·H20
CD端产物的判断n(H2O)=(6.52-5.44)÷18=0.06mol,结晶水全部失去,产物化学式为CaS04
最后为氧化钙
考点:考查实验探究中流程的控制、分析等有关问题。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
实验室中制取、洗气并收集气体的装置如图所示。仅用此该装置和表中提供的物质完成相关实验,最合理的选项是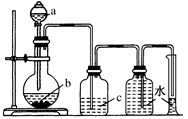
| 选项 | a中的液体 | b中的固体 | c中液体 |
| A | 浓盐酸 | MnO2 | 饱和食盐水 |
| B | 浓氨水 | 生石灰 | 浓H2SO4 |
| C | 浓硫酸 | Cu片 | NaOH溶液 |
| D | 稀HNO3 | Cu片 | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,应加热蒸馏,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是( )
| A.产品中有被蒸馏出的H2SO4 |
| B.有部分未反应的乙酸被蒸馏出来 |
| C.有部分未反应的乙醇被蒸馏出来 |
| D.有部分乙醇跟浓H2SO4作用生成乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。钙在加热时能与氮气、氢气反应。氢化钙遇水立即反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,下图是模拟制取装置。
(1)下列关于氢化钙的叙述正确的是 (选填序号)。
a.氢化钙中阴离子的半径小于Li+的半径
b.氢化钙的式量小于溴化氢,因此前者的熔点小于后者
c.氢化钙也能与盐酸反应生成氢气
d.氢气常用作还原剂,只具有还原性
(2)上图A装置中制备氢气所用的酸溶液最好选用 (选填序号)。
a.稀盐酸 b.稀硫酸 c.稀硝酸 d.均可以
(3)装置D中竖直导管的作用是 。
(4)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是 。加热C装置前要对H2验纯,验纯的操作是 。
(5)甲同学认为只要装置合理、操作规范就可以排除生成 (选填序号)。
a.Ca3N2 b.CaO c.Ca(OH)2
(6)乙同学用下图装置测定制得的氢化钙的纯度。他称取48g样品,与足量的水反应,恒温时,注射器量出产生的气体为48.16 L(已换算为标准状况)。假设钙只与氢气发生了反应,请根据乙同学的实验数据计算氢化钙的纯度(写出计算过程) 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯气和氮氧化物都是重要的化工原料,但进入大气后,都对环境造成污染。
【Ⅰ】已知:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+ 8 H2O,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是 。(选填A或B或C)
(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式: 。
(3)常用NaOH溶液吸收氯气防止污染。写出该反应的离子方程式 。
【Ⅱ】已知:NO2+NO+2NaOH=2NaNO2+H2O,可用氢氧化钠溶液可以吸收废气中的氮氧化物。
(1)在该反应中,氧化剂是 。
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气无污染的物质。写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有A、B、C、D、E、F六种物质,它们之间相互转化关系如图所示(条件及部分产物未标出)。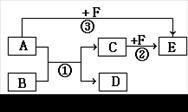
(1)若A、D为气体,都能使澄清的石灰水变浑浊;B、F做焰色反应,透过蓝色钴玻璃观察为紫色, B、C为正盐,F的溶液为紫红色。则C和F在酸性溶液中发生反应②的离子方程式为 。
(2)若1 mol A分子中含有3 mol极性共价键, B、C、F都是短周期元素组成的非金属单质;常温下,只有D为固体,其它为气体。则反应③的化学方程式为 。
某同学设计了如图所示装置(夹持仪器省略)进行上述(2)中物质B的化学性质探究。
①你认为此装置设计是否合理?若不合理如何改进: 。(若合理此问不答)
②Ⅱ中产生的现象是 。
③反应几分钟后,检验Ⅲ中可能含有的金属阳离子的实验操作是 。
④通过以上探究,气体B的主要化学性质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)黄铜矿是工业炼铜的主要原料,主要成分为CuFeS2,含少量脉石。为测定该黄铜矿的纯度,某同学设计了如下实验:
用电子天平称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准碘溶液20.00mL。请回答下列问题:
(1)将样品研细后再进行反应,其目的是 ;标准碘溶液应盛放在(填“碱式”或“酸式”) 滴定管中。
(2)装置a的作用是
(填序号)。
| A.除去空气中的二氧化碳 | B.除去空气中的水蒸气 |
| C.有利于气体混合 | D.有利于观察、控制空气流速 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com