
【题目】12.8 g铜和浓HNO3反应,随反应进行,产生气体的颜色逐渐变浅,铜完全反应时,收集到标准状况下的气体6.72 L,将气体与一定体积的O2同时通入水中可被完全吸收。
(1)通过计算确定收集到的气体成分及物质的量。
(2)O2在标准状况下的体积。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾。
(1)SO2和O2反应制取SO3的反应原理为:2SO2+O2![]() 2SO3,经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
2SO3,经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
① 则这段时间为_______s。
② 该反应达到平衡状态的标志是_______。
A.容器内硫元素物质的量分数不变 B.混合物的平均相对分子质量不变
C.n(SO2):n(O2):n(SO3)=2:1:2 D.各组分的体积分数不变
(2)利用烧渣制绿矾的过程如下:
![]()
操作I的名称____________,溶液A的溶质___________,固体B是__________。
(3)某科研机构用NaOH溶液吸收废气中的SO2,将所得的Na2SO4溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示,(电极材料为石墨)

① 图中b极要连接电源的___________极(填“正”或“负” )
②SO32-放电的电极反应式为__________。
③ 若用甲烷-空气燃料电池作电源,处理标准状况下40m3的废气(其中SO2的体积分数为0.2 ) ,理论上需要消耗标准状况下甲烷___________m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)化合物H是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:
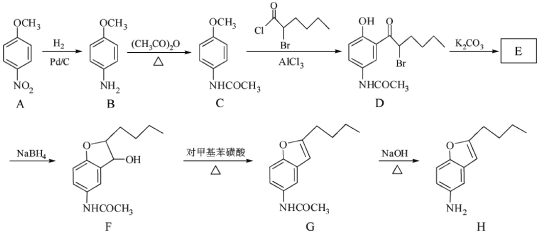
(1)D中的含氧官能团名称为____________(写两种)。
(2)F→G的反应类型为___________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_________。
①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(4)E经还原得到F,E的分子是为C14H17O3N,写出E的结构简式:___________。
(5)已知:①苯胺(![]() )易被氧化
)易被氧化
②
请以甲苯和(CH3CO)2O为原料制备 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃X完全燃烧时,生成的n(H2O)=n(CO2),X不能使溴水褪色。X的分子式可能是
A.C2H2 B.C2H4 C.C3H4 D.C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,并检验反应的部分副产物和探究溴乙烷的性质。已知:NaBr+H2SO4![]() NaHSO4+HBr↑
NaHSO4+HBr↑
(一)溴乙烷的制备及产物的检验:设计了下图装置,其中夹持仪器、加热仪器及冷水管没有画出。请根据实验步骤,回答下列问题:

(1)制备操作中,加入少量的水,其目的是 (填字母)。
a.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
(2)检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验。B、C中应盛放的试剂分别是 、 (填字母)。
a.苯 b.水 c.NaOH 溶液 d.硝酸银溶液
(3)欲除去溴乙烷中的少量杂质Br2,正确方法是 (填字母)。
a.KI溶液洗涤
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
(二)溴乙烷性质的探究:某同学用下图装置(铁架台、酒精灯等未画出)来探究溴乙烷的性质。在试管中加入10 mL 6molL-1NaOH水溶液和5 mL 溴乙烷,水浴加热。当观察到___________ 现象时,表明溴乙烷与NaOH水溶液已完全反应。该反应的化学方程式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)毗氟氯禾灵的合成路线如下:

已知:![]()
(1)B的结构简式为_____________。A的系统名称为_____________。
(2)在合成吡氟氯禾灵所涉及的反应中,属于加成反应的有___________(填序号)。
(3)写出反应⑥的化学方程式___________________。
(4)C的同分异构体有多种,写出同时具有下列性质的同分异构体的结构简式___________________。
a.能与FeCl3溶液发生显色反应 b.能发生银镜反应 c.核磁共振氢谱图中有四组峰
(5)写出由![]() 制备高分子化合物
制备高分子化合物![]() 的合成路线流程图(无机试剂任选),合成流程示意图如下:
的合成路线流程图(无机试剂任选),合成流程示意图如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,则该温度下水的KW=_______。在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,若所得混合液为中性,且a+b=12,则Va:Vb=___________。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是___________(填“强电解质”或“弱电解质”)。
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是__________(填字母)
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显__________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X2-与Y+离子都与Ar原子具有相同的核外电子排布,则下列叙述中正确的是
A. 原子序数X>Y
B. 离子半径X>Y
C. X和Y一定在同一周期
D. X是第IIA族元素,Y是第VIIA族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(化学式为:Na2S2O5):白色粉末,水溶液显酸性,受潮易分解,遇强酸则放出一种刺激性气味的气体。它是一种化工原料,常用作抗氧化剂。
工业上,常用湿法制作焦亚硫酸钠,湿法制作有三步,其中:
第一步:在饱和碳酸钠溶液中通入足量的SO2,调至PH=4.1,得亚硫酸氢钠;
第二步:……
第三步:……
根据上述内容,回答问题:
(1)焦亚硫酸钠中S的化合价为
(2)第一步化学方程式为:
(3)焦亚硫酸钠含量测定:取焦亚硫酸钠样品约0.15g ,于密封瓶中,加入0.05mol/L碘(I2)滴定液50ml,塞紧,振摇溶解后,加盐酸1ml,用0.1mol/L硫代硫酸钠(Na2S2O3)滴定液滴定,至近终点时,加淀粉指示液2ml,继续滴定至蓝色消失,用去硫代硫酸钠溶液VmL。并将滴定结果进行空白对比。
已知:每1ml碘滴定液(0.05mol/L)相当于4.750mg的Na2S2O5。
该反应有两个离子方程式,分别为:
a: 3H2O + S2O52- + 2I2 = 2SO42- + 4I- + 6H+
b: 5H2O + S2O32- + 4I2 = 2SO42- + 8I- + 10H+
①a反应中每消耗1mol还原剂转移 mol电子;
②滴定至终点时的判定方法是: ;
③焦亚硫酸钠的质量分数为(列式表示,不计算结果): (可能用到的相对分子质量:Na2S2O5=190)
④由于碘单质在水中溶解度低,因此碘滴定液通常用I2与KI混溶得到碘(KI3)滴定液。取12.7g碘单质和26.6g碘化钾加水50mL溶解后,加盐酸3滴,定容至1000mL。该碘(KI3)滴定液物质的量浓度为 ;该碘(KI3)滴定液与焦亚硫酸钠反应时具有 性(填“氧化”或“还原”)。[可能用到的相对原子质量:I=127、K=39]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com