
”¾ĢāÄæ”æ»·¾³ĪŹĢāŌ½Ą“Ō½ŹÜµ½ČĖĆĒµÄÖŲŹÓ£¬ŃŠ¾æ±ķĆ÷µŖŃõ»ÆĪļŗĶ¶žŃõ»ÆĮņŌŚŠĪ³ÉĪķö²Ź±Óė“óĘųÖŠµÄ°±ÓŠ¹Ų£ØČēĶ¼ĖłŹ¾£©”£

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©![]() µÄµē×ÓŹ½ĪŖ____________£¬
µÄµē×ÓŹ½ĪŖ____________£¬![]() ÖŠŗ¬ÓŠµÄ»Æѧ¼üŹĒ____________”£
ÖŠŗ¬ÓŠµÄ»Æѧ¼üŹĒ____________”£
£Ø2£©ĻĀĮŠ¹ŲÓŚĪķö²µÄŠšŹö“ķĪóµÄŹĒ______£ØĢīŠņŗÅ£©£ŗ
A£®Īķö²ÖŠŗ¬ÓŠĻõĖįļ§ŗĶĮņĖįļ§ B£®![]() ŹĒŠĪ³ÉĪŽ»śæÅĮ£ĪļµÄ“߻ƼĮ
ŹĒŠĪ³ÉĪŽ»śæÅĮ£ĪļµÄ“߻ƼĮ
C£®Īķö²µÄŠĪ³ÉÓė¹ż¶ČŹ©ÓƵŖ·ŹÓŠ¹Ų D£®Īķö²µÄŠĪ³É¹ż³ĢÉę¼°Ńõ»Æ»¹Ō·“Ó¦
£Ø3£©Ō¤·Ąŗ¬Įņ»ÆŗĻĪļĪķö²Éś³ÉµÄ·½·ØÖ®Ņ»ŹĒ½«°±ĘųŗĶ¶žŃõ»ÆĮņĶØČėĖ®ÖŠ£¬ŌŁ³äČė![]() ³ä·Ö·“Ӧɜ³ÉŅ»ÖÖÕżŃĪ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
³ä·Ö·“Ӧɜ³ÉŅ»ÖÖÕżŃĪ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
£Ø4£©ŌŚÓŠŃõĢõ¼žĻĀ£¬“߻ƼĮÄÜ“ß»Æ![]() Óė
Óė![]() ·“Ӧɜ³É
·“Ӧɜ³É![]() ”£½«Ņ»¶Ø±ČĄżµÄ
”£½«Ņ»¶Ø±ČĄżµÄ![]() ”¢
”¢![]() ŗĶ
ŗĶ![]() »ģŗĻĘųĢåŌČĖŁĶØČė×°ÓŠ“߻ƼĮµÄ·“Ó¦Ę÷ÖŠ·“Ó¦£¬²āµĆ·“Ó¦ĪĀ¶ČøßÓŚ380”ꏱ£¬
»ģŗĻĘųĢåŌČĖŁĶØČė×°ÓŠ“߻ƼĮµÄ·“Ó¦Ę÷ÖŠ·“Ó¦£¬²āµĆ·“Ó¦ĪĀ¶ČøßÓŚ380”ꏱ£¬![]() µÄČ„³żĀŹŃøĖŁĻĀ½µ£¬ĘäŌŅņÖ®Ņ»ŹĒ“߻ƼĮ»īŠŌĻĀ½µ£¬ĮķŅ»ÖŲŅŖŌŅņŹĒ____________”£ŌŚĪŽŃõĢõ¼žĻĀ£¬·“Ó¦Ę÷ÖŠ
µÄČ„³żĀŹŃøĖŁĻĀ½µ£¬ĘäŌŅņÖ®Ņ»ŹĒ“߻ƼĮ»īŠŌĻĀ½µ£¬ĮķŅ»ÖŲŅŖŌŅņŹĒ____________”£ŌŚĪŽŃõĢõ¼žĻĀ£¬·“Ó¦Ę÷ÖŠ![]() Äܽ«
Äܽ«![]() »¹ŌĪŖ
»¹ŌĪŖ![]() £¬µ±Éś³É
£¬µ±Éś³É![]() Ź±×ŖŅʵē×Ó______
Ź±×ŖŅʵē×Ó______![]() £ØæÉÓĆ·ÖŹż±ķŹ¾£©”£
£ØæÉÓĆ·ÖŹż±ķŹ¾£©”£
”¾“š°ø”æ![]() ¹²¼Ū¼üŗĶĄė×Ó¼ü B
¹²¼Ū¼üŗĶĄė×Ó¼ü B ![]()
![]() Óė
Óė![]() ·“Ӧɜ³ÉĮĖ
·“Ӧɜ³ÉĮĖ![]()
![]()
”¾½āĪö”æ
£Ø1£©NH3·Ö×ÓÖŠµÄNŗĶ3øöH·Ö±šŠĪ³É¹²¼Ū¼ü£¬Ź¹Ö®“ļµ½8µē×ÓŗĶ2µē×ÓĪČ¶Ø½į¹¹£¬N”¢H£¬N”¢OÖ®¼äŹĒ¹²¼Ū¼ü¶ųNH4+ŗĶNO3-Ö®¼äŹĒĄė×Ó¼ü£»
£Ø2£©ŅĄ¾Ż×Ŗ»ÆĶ¼£¬æÉ·ÖĪöĪķö²µÄ×é³É£¬¼°×Ŗ»Æ¹ż³ĢÖŠĖł·¢ÉśµÄ·“Ó¦ĄąŠĶ£»
£Ø3£©½«°±ĘųŗĶ¶žŃõ»ÆĮņĶØČėĖ®ÖŠ£¬ŌŁ³äČėŃõĘų³ä·Ö·“Ӧɜ³ÉĮņĖįļ§£»
£Ø4£©NH3¾ßÓŠ»¹ŌŠŌ£¬O2¾ßÓŠŃõ»ÆŠŌ£¬ĪĀ¶ČøßÓŚ380”ꏱ£¬NH3ŗĶO2·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Éś³ÉNO£¬ĒŅĻūŗÄĮĖO2£¬ĖłŅŌµ¼ÖĀNOxµÄČ„³żĀŹŃøĖŁĻĀ½µ£¬ŌŚĪŽŃõĢõ¼žĻĀ£¬NH3ŗĶNO2·“ÉśŃõ»Æ»··“Ó¦£ŗ8NH3![]() 6NO2
6NO2![]() 7N2
7N2![]() 12H2O£¬ŅŌ“Ė½ā“š£»
12H2O£¬ŅŌ“Ė½ā“š£»
£Ø1£©NH3·Ö×ÓÖŠµÄNŗĶ3øöH·Ö±šŠĪ³É¹²¼Ū¼ü£¬Ęäµē×ÓŹ½ĪŖ£ŗ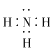 £¬NH4NO3ŹĒĄė×Ó»ÆŗĻĪļ£¬NH4+ŗĶNO3-Ö®¼äŹĒĄė×Ó¼ü£¬NH4+ŗĶNO3-ÖŠŗ¬ÓŠ¹²¼Ū¼ü£¬¹ŹNH4NO3¼ČÓŠĄė×Ó¼üÓÖÓŠ¹²¼Ū¼ü£»
£¬NH4NO3ŹĒĄė×Ó»ÆŗĻĪļ£¬NH4+ŗĶNO3-Ö®¼äŹĒĄė×Ó¼ü£¬NH4+ŗĶNO3-ÖŠŗ¬ÓŠ¹²¼Ū¼ü£¬¹ŹNH4NO3¼ČÓŠĄė×Ó¼üÓÖÓŠ¹²¼Ū¼ü£»
±¾Ģā“š°øĪŖ£ŗ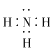 £¬¹²¼Ū¼üŗĶĄė×Ó¼ü”£
£¬¹²¼Ū¼üŗĶĄė×Ó¼ü”£
£Ø2£©A.ÓÉÓŚµŖµÄŃõ»ÆĪļ”¢¶žŃõ»ÆĮņ×Ŗ»ÆĪŖļ§ŃĪ£¬ŠĪ³ÉĪŽ»śæÅĮ£Īļ£¬ÓÉ“ĖæÉÖŖĪķö²ÖŠŗ¬ÓŠĻõĖįļ§ŗĶĮņĖįļ§£¬¹ŹAÕżČ·£»
B.“߻ƼĮŹĒÖøÄÜøıä»Æѧ·“Ó¦ĖŁĀŹ£¬¶ų±¾ÉķŌŚ»Æѧ·“Ó¦Ē°ŗóÖŹĮæŗĶ»ÆѧŠŌÖŹ¶¼²»·¢ÉśøıäµÄĪļÖŹ”£¶ųNH3²Ī¼ÓĮĖ·“Ó¦×Ŗ»Æ³ÉĮĖļ§ŃĪ£¬ĖłŅŌNH3²»ŹĒŠĪ³ÉĪŽ»śæÅĮ£µÄ“߻ƼĮ£¬¹ŹB“ķĪó£»
C. ÓÉÓŚµŖµÄŃõ»ÆĪļ”¢¶žŃõ»ÆĮņ×Ŗ»ÆĪŖļ§ŃĪ£¬ŌŚ“Ė¹ż³ĢÖŠÓė“óĘųÖŠµÄNH3ÓŠ¹Ų£¬ÓÉÓŚµŖ·Ź»įŹĶ·Å°±Ęų£¬ĖłŅŌĪķö²µÄŠĪ³ÉÓė¹ż¶ČŹ©ÓƵŖ·ŹÓŠ¹Ų£¬¹ŹCÕżČ·£»
D.Īķö²µÄŠĪ³É¹ż³ĢÖŠ£¬ÓÉNOx![]() NO5£¬SO2
NO5£¬SO2![]() SO3¾łŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹDÕżČ·£»
SO3¾łŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹDÕżČ·£»
±¾Ģā“š°øĪŖ£ŗB”£
£Ø3£©½«°±ĘųŗĶ¶žŃõ»ÆĮņĶØČėĖ®ÖŠ£¬ŌŁ³äČėO2³ä·Ö·“Ӧɜ³ÉĮņĖįļ§£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ4NH3![]() 2SO2
2SO2![]() O2
O2![]() 2H2O=2£ØNH4£©2SO4£»
2H2O=2£ØNH4£©2SO4£»
±¾Ģā“š°øĪŖ£ŗ4NH3![]() 2SO2
2SO2![]() O2
O2![]() 2H2O=2£ØNH4£©2SO4”£
2H2O=2£ØNH4£©2SO4”£
£Ø4£©NH3¾ßÓŠ»¹ŌŠŌ£¬O2¾ßÓŠŃõ»ÆŠŌ£¬ĪĀ¶ČøßÓŚ380”ꏱ£¬NH3ŗĶO2·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬4NH3![]() 5O2
5O2![]() 4NO
4NO![]() 6H2O£¬Éś³ÉNO£¬ĒŅĻūŗÄĮĖO2£¬ĖłŅŌµ¼ÖĀNOxµÄČ„³żĀŹŃøĖŁĻĀ½µ£»ŌŚĪŽŃõĢõ¼žĻĀ£¬NH3ŗĶNO2·“ÉśŃõ»Æ»··“Ó¦£ŗ8NH3
6H2O£¬Éś³ÉNO£¬ĒŅĻūŗÄĮĖO2£¬ĖłŅŌµ¼ÖĀNOxµÄČ„³żĀŹŃøĖŁĻĀ½µ£»ŌŚĪŽŃõĢõ¼žĻĀ£¬NH3ŗĶNO2·“ÉśŃõ»Æ»··“Ó¦£ŗ8NH3![]() 6NO2
6NO2![]() 7N2
7N2![]() 12H2O£¬øĆ·“Ó¦ÖŠNH3ÖŠµÄN»ÆŗĻ¼Ū-3
12H2O£¬øĆ·“Ó¦ÖŠNH3ÖŠµÄN»ÆŗĻ¼Ū-3![]() 0£¬NO2ÖŠNµÄ»ÆŗĻ¼Ū+4
0£¬NO2ÖŠNµÄ»ÆŗĻ¼Ū+4![]() 0£¬Éś³É7molN2×ŖŅĘ24molµē×Ó,ĖłŅŌÉś³É1molN2×ŖŅʵē×Ó24/7mol£»
0£¬Éś³É7molN2×ŖŅĘ24molµē×Ó,ĖłŅŌÉś³É1molN2×ŖŅʵē×Ó24/7mol£»
±¾Ģā“š°øĪŖ£ŗNH3ŗĶO2Éś³ÉĮĖNO£¬24/7”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗćĪĀ”¢ŗćČŻµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ·“Ó¦A(g)£«B(g)![]() C(g)£¬Čō·“Ó¦ĪļAµÄÅØ¶Č“Ó2 mol”¤L£1½µµ½0.8 mol”¤L£1Šč20 s£¬Ōņ·“Ó¦ĪļAµÄÅضČÓÉ0.8 mol”¤L£1½µµ½0.2 mol”¤L£1ĖłŠčµÄ·“Ó¦Ź±¼ä( )
C(g)£¬Čō·“Ó¦ĪļAµÄÅØ¶Č“Ó2 mol”¤L£1½µµ½0.8 mol”¤L£1Šč20 s£¬Ōņ·“Ó¦ĪļAµÄÅضČÓÉ0.8 mol”¤L£1½µµ½0.2 mol”¤L£1ĖłŠčµÄ·“Ó¦Ź±¼ä( )
A. µČÓŚ10 sB. “óÓŚ10 sC. Š”ÓŚ10 sD. ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ¶”“¼£ØC4H10O)ŗĶ¼ŗĻ©£ØC6H12)×é³ÉµÄ»ģŗĻĪļÖŠ£¬ĘäÖŠŃõŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ8%£¬ŌņĒāŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ£Ø £©
A. 13%B. 14%C. 26%D. ĪŽ·Ø¼ĘĖć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ·ÖĄąµÄÕżČ·×éŗĻŹĒ
Ń”Ļī | »ģŗĻĪļ | »ÆŗĻĪļ | µ„ÖŹ | ŃĪ |
A | ŃĪĖį | NaOH¹ĢĢå | ŹÆÄ« | Ź³ŃĪ |
B | ¼īŹÆ»Ņ | ½šøÕŹÆ | O3 | “æ¼ī(Na2CO3) |
C | æÕĘų | ³ĪĒåŹÆ»ŅĖ® | Ģś | ŹÆ»ŅŹÆ |
D | CuSO4”¤5H2O | CaCl2 | Ė®Ņų | CaO |
A. AB. BC. CD. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ĖłŹ¾µÄµē½ā³ŲIŗĶIIÖŠ£¬a”¢b”¢cŗĶd¾łĪŖPtµē¼«”£µē½ā¹ż³ĢÖŠ£¬µē¼«bŗĶdÉĻƻӊĘųĢåŅŻ³ö£¬µ«ÖŹĮæ¾łŌö“ó£¬ĒŅŌöÖŲb>d”£·ūŗĻÉĻŹöŹµŃé½į¹ūµÄŃĪČÜŅŗŹĒ

Ń”Ļī | X | Y |
A£® | MgSO4 | CuSO4 |
B£® | AgNO3 | CuSO4 |
C£® | FeSO4 | Al2(SO4)3 |
D£® | CuSO4 | AgNO3 |
A. AB. BC. CD. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĆæ×éĪļÖŹ·¢ÉśĖłŹö±ä»ÆæĖ·žµÄ×÷ÓĆŹōÓŚĶ¬ÖÖĄąŠĶµÄŹĒ£Ø £©
A.ĀČ»ÆĀĮŗĶøɱłÉż»ŖB.ÄĘŗĶĮņČŪ»Æ
C.Ź³ŃĪŗĶĀČ»ÆĒāČܽāÓŚĖ®D.¶žŃõ»Æ¹čŗĶ¶žŃõ»ÆĮņČŪ»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖŃõ»ÆĀĮ(AlON)ŹōÓŚŌ×Ó¾§Ģ壬ŹĒŅ»ÖÖ³¬ĒæĶøĆ÷²ÄĮĻ£¬ĻĀĮŠĆčŹö“ķµÄŹĒ(””””)
A.AlONŗĶŹÆÓ¢µÄ»Æѧ¼üĄąŠĶĻąĶ¬B.µē½āČŪČŚAlONæɵƵ½Al
C.AlONµÄNŌŖĖŲ»ÆŗĻ¼ŪĪŖ©1D.AlONŗĶŹÆÓ¢¾§ĢåĄąŠĶĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚ»Æ¹¤Éś³ÉµČĮģÓņÓ¦ÓĆ¹ć·ŗ”£
£Ø1£©¹¤ŅµĪ²ĘųÖŠµÄSO2Ņ»Ö±ŹĒ»·¾³ĪŪČ¾µÄÖ÷ŅŖŌŅņÖ®Ņ»£¬¹¤ŅµÉĻ³£²ÉÓĆČēĻĀ·½·Ø½µµĶĪ²ĘųÖŠµÄŗ¬ĮņĮæ£ŗ
¢Ł·½·Ø1£ŗČ¼ĆŗÖŠ¼ÓČėÉśŹÆ»Ņ£¬½«SO2×Ŗ»ÆĪŖCaSO3£¬ŌŁŃõ»ÆĪŖCaSO4
ŅŃÖŖ£ŗa. CaO(s)+CO2(g) =CaCO3(s) ¦¤H=-178.3kJ”¤mol-1
b.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g) ¦¤H=-2762.2kJ”¤mol-1
c.2CaSO3(s)+O2(g)=2CaSO4(s) ¦¤H=-2314.8kJ”¤mol-1
Š“³öCaO(s)ÓėSO2(g)·“Ӧɜ³ÉCaSO3(s)µÄČČ»Æѧ·½³ĢŹ½£ŗ____________________________”£
¢Ś·½·Ø2£ŗÓĆĒāŃõ»ÆÄĘČÜŅŗ½«SO2×Ŗ»ÆĪŖNaHSO3£¬ŌŁŃõ»ÆĪŖ Na2SO4”£ŹµŃé²āµĆNaHSO3ČÜŅŗÖŠ![]() = 1500£¬ŌņČÜŅŗµÄpHĪŖ______________£ØŅŃÖŖ£ŗH2SO3µÄKa1=1.5”Į10-2£¬Ka2=1.0”Į10-7£©”£
= 1500£¬ŌņČÜŅŗµÄpHĪŖ______________£ØŅŃÖŖ£ŗH2SO3µÄKa1=1.5”Į10-2£¬Ka2=1.0”Į10-7£©”£
£Ø2£©ĆŗÖĘµĆµÄ»Æ¹¤ŌĮĻĘųÖŠŗ¬ÓŠōŹ»łĮņ(0=C=S)£¬øĆĪļÖŹæÉ×Ŗ»ÆĪŖH2S£¬·“Ó¦ĪŖCOS(g) +H2(g)![]() H2S (g)+CO(g) ¦¤H>0”£
H2S (g)+CO(g) ¦¤H>0”£
¢ŁŗćĪĀŗćČŻĢõ¼žĻĀ£¬ĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ĻĀĮŠŹĀŹµ²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ__________(Ģī×ÖÄø)”£
a.COSµÄÅØ¶Č±£³Ö²»±ä b.»ÆŃ§Ę½ŗā³£Źż²»ŌŁøıä
c.»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıä d.ŠĪ³É2molH-S¼üµÄĶ¬Ź±ŠĪ³É1mol H-H¼ü
¢ŚT1”ꏱ£¬ŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ£¬½«Ņ»¶ØĮæµÄCOŗĶH2S»ģŗĻ¼ÓČČ²¢“ļµ½ĻĀĮŠĘ½ŗā£ŗH2S(g)+ CO(g) ![]() COS(g)+H2(g)£¬K=0.25£¬ŌņøĆĪĀ¶ČĻĀ·“Ó¦COS(g)+H2(g)
COS(g)+H2(g)£¬K=0.25£¬ŌņøĆĪĀ¶ČĻĀ·“Ó¦COS(g)+H2(g)![]() H2S(g)+ CO(g)µÄĘ½ŗā³£ŹżK=__________”£T1”ꏱ£¬ĻņČŻ»żĪŖ10 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1mol COS(g)ŗĶ1molH2(g)£¬“ļµ½Ę½ŗāŹ±COSµÄ×Ŗ»ÆĀŹĪŖ______________________”£
H2S(g)+ CO(g)µÄĘ½ŗā³£ŹżK=__________”£T1”ꏱ£¬ĻņČŻ»żĪŖ10 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1mol COS(g)ŗĶ1molH2(g)£¬“ļµ½Ę½ŗāŹ±COSµÄ×Ŗ»ÆĀŹĪŖ______________________”£
£Ø3£©¹ż¶žĮņĖį(H2S2O8)ŹĒŅ»ÖÖĒæŃõ»ÆŠŌĖį£¬Ęä½į¹¹Ź½ĪŖ
 ӣ
ӣ
¢ŁŌŚAg+“ß»Æ×÷ÓĆĻĀ£¬S2O82-ÄÜÓėMn2+ŌŚĖ®ČÜŅŗÖŠ·¢Éś·“Ӧɜ³ÉSO42-ŗĶMnO4-£¬1mol S2O82-ÄÜŃõ»ÆµÄMn2+µÄĪļÖŹµÄĮæĪŖ_________mol”£
¢Ś¹¤ŅµÉĻæÉÓƶčŠŌµē¼«µē½āĮņĖįŗĶĮņĖįļ§»ģŗĻČÜŅŗÖʱø¹ż¶žĮņĖįļ§”£ŌņŃō¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÕĘų“µ³ö·Ø¹¤ŅÕŹĒÄæĒ°”°ŗ£Ė®Ģįäå”±µÄ×īÖ÷ŅŖ·½·ØÖ®Ņ»”£Ę乤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£¬ĘäÖŠ²»ÕżČ·µÄŹĒ

A£®²½Öč¢Ü¢ŻŹĒĪŖĮĖø»¼Æäå
B£®²½Öč¢ŪĖµĆ÷äå¾ßÓŠ»Ó·¢ŠŌ
C£®²½Öč¢ÜµÄĄė×Ó·½³ĢŹ½ĪŖBr2+SO2+H2O![]() 2H++2Br-+SO32-
2H++2Br-+SO32-
D£®²½Öč¢ąÖŠäåÕōĘųĄäÄżŗóµĆµ½ŅŗäåÓėäåĖ®µÄ»ģŗĻĪļæÉÓĆ·ÖŅŗĀ©¶··ÖĄė
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com