
下列有关物质的性质和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验Cl2管道是否泄漏
B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
C.碳酸氢钠热稳定性弱,用作焙制糕点的发酵粉
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
科目:高中化学 来源: 题型:
在一个绝热容器中,放入Ca(OH)2悬浊液,有平衡:
Ca(OH)2(s) 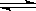 Ca2+(aq)+2OH-(aq)ΔH<0 。
Ca2+(aq)+2OH-(aq)ΔH<0 。
已知:CaO(s)+H2O(l) = Ca(OH)2(s)ΔH<0 。下列说法正确的是( )
A.向溶液中加少量CaO,达新平衡后,溶液的pH不变
B.向溶液中加少量CaO,达新平衡后,溶液的pH降低
C.向溶液中加入Na2CO3溶液,其中Ca(OH)2固体质量增加
D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如下:

(1)已知(NH4)2Ce(NO3)6受热易分解,某科研小组认为反应原理如下,请补充完整:(NH4)2Ce(NO3)6 CeO2·8OH + 8_____↑;CeO2·8OH
CeO2·8OH + 8_____↑;CeO2·8OH CeO2+ 4H2O↑+2O2↑。
CeO2+ 4H2O↑+2O2↑。
在空气中加热(NH4)2Ce(NO3)6,除固体颜色有变化外,还可观察到的现象是_________。
(2)步骤Ⅰ中,将Ce(NO3)3·6H2O配成溶液,保持pH到4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀。该过程中参加反应的氧化剂与还原剂物质的量之比为___________。
(3)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=___________。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10—5mol·L-1,需调节pH为______以上。
 (4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如右图。从图中可得出三条主要规律:
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如右图。从图中可得出三条主要规律:
① (NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
② _____________________________________________;
③ _____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
CPAE是蜂胶的主要活性成分,也可由咖啡酸合成:
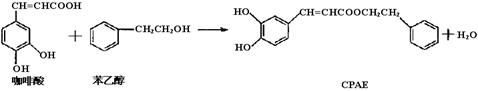
下列说法不正确的是
A.咖啡酸分子中所有原子可能处在同一个平面上
B.可用金属Na检测上述反应是否残留苯乙醇
C.1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写不正确的是
A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+ )=7:2时:
2Al3+ + 7OH - = Al(OH)3↓+ AlO2- + 2H2O
B.氨水吸收足量的SO2气体:NH3·H2O+SO2=NH4+ + HSO3-
C.高锰酸钾酸性溶液与草酸溶液反应:
2MnO4-+ 5C2O42- + 16H+ = 2Mn2+ + 10CO2↑+ 8H2O
D.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+= Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列四个图像的说法中正确的是( )

A. 图①t1时改变的条件可能是升高了温度或增大了压强
B. 图②该微粒仅为18O2-不能为16O2-
C. 图③若A为CaO,则B可能为MgO
D. 图④中的ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于加成反应的是
A.甲烷与氯气的混合气体在光照条件下的反应
B.丙烯和氯气在一定条件下生成ClCH2CH=CH2的反应
C.乙烯使酸性高锰酸钾溶液褪色的反应
D.乙烯与溴水的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿佛加德罗常数,下列说法正确的是( )
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.14g氮气中含有7NA个电子
C.在25℃,101kPa时,22.4L氢气中含有2NA个氢原子
D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7 :4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com