
| 实验操作 | 结论 | |
| A | 乙醇、浓硫酸混合加热170℃,导出的物质能使酸性高锰酸钾褪色 | 该反应生成了乙烯 |
| B | 在溴乙烷中加入适量的氢氧化钠溶液,加热一段时间,再滴入几滴硝酸银,会有沉淀析出 | 溴乙烷在碱性条件下能水解出Br- |
| C | 提纯粗苯甲酸用重结晶法,主要步骤为:加热溶解、趁热过滤、冷却结晶、过滤、洗涤 | 苯甲酸在水中的溶解度受温度影响很大 |
| D | 可用裂化汽油萃取溴水中的溴,且将有机层从分液漏斗上口倒出 | 裂化汽油密度比水小 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生消去反应生成乙烯,乙醇易挥发,乙醇、乙烯均能被高锰酸钾氧化;
B.溴乙烷中加入适量的氢氧化钠溶液,发生水解反应,检验溴离子,应在酸性条件下;
C.溶解后,趁热过滤减少苯甲酸的损失;
D.裂化汽油含碳碳双键,与溴水发生加成反应.
解答 解:A.发生消去反应生成乙烯,乙醇易挥发,乙醇、乙烯均能被高锰酸钾氧化,则高锰酸钾褪色,不能说明乙烯的生成,故A错误;
B.溴乙烷中加入适量的氢氧化钠溶液,发生水解反应,检验溴离子,应在酸性条件下,没有加硝酸至酸性,不能检验,故B错误;
C.因苯甲酸在水中的溶解度受温度影响很大,溶解后,趁热过滤减少苯甲酸的损失,冷却结晶、过滤、洗涤可提纯粗苯甲酸,故C正确;
D.裂化汽油含碳碳双键,与溴水发生加成反应,不能作萃取剂,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、有机反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L甲烷、戊烷混合物所含分子数为0.1NA | |
| B. | 0.1molC2H6O分子中含有的C-H的数目一定为0.5NA | |
| C. | 1L lmol/L的CH3COONa溶液中所含CH3COO-个数为0.1NA | |
| D. | 标准状况下,2.24L16O2和3.6g18O2含有氧原子均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | KMnO4溶液的浓度(mol•L-1) | KMnO4溶液滴入的体积(mL) |
| 1 | 0.0200 | V1=20.02 |
| 2 | 0.0200 | V2=20.12 |
| 3 | 0.0200 | V3=19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
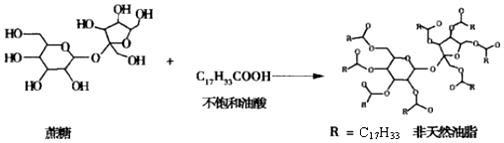
| A. | 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象 | |
| B. | 天然油脂、蔗糖、非天然油脂都能发生水解反应 | |
| C. | 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应 | |
| D. | 植物油、非天然油脂都可以与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒温恒容时,混合气体颜色不再变化 | |
| B. | 一个H-H 键断裂的同时有两个H-I键断裂 | |
| C. | 恒温、压强一定,体积可变的容器,混合气体的密度不再变化 | |
| D. | 恒温恒容时,某一生成物浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的 | |
| B. | 葡萄糖和蔗糖不是同分异构体,但属于同系物 | |
| C. | 所有蛋白质均可通过颜色反应来鉴别 | |
| D. | 油脂在酸性条件下水解生成丙三醇和高级脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精溶于水 | B. | 水冻成冰 | ||
| C. | 氯化钠受热熔化 | D. | 氧化钙作为干燥剂吸水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体压强保持不变 | |
| B. | 吸收y mol H2只需1 mol MHx | |
| C. | 若降温,该反应的平衡常数减小 | |
| D. | 若向容器内通入少量氢气,则v(放氢)>v(吸氢) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com