
【题目】A、B都是芳香族化合物,![]() 水解得到
水解得到![]() 和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使氯化铁溶液显色。
和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使氯化铁溶液显色。
(1)A、B相对分子质量之差为____________________。
(2)1个B中应该有____________________个氧原子。
(3)A的分子式为____________________。
【答案】42 3 ![]()
【解析】
A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且B分子碳和氢元素总的质量百分含量为65.2%,根据B+CH3COOH→A+H2O判断,假设A的相对分子质量为200,则B的最大相对分子质量为156,含氧34.8%,则氧原子个数为![]() ≈3,即B分子中含有3个O原子,则有机物B的相对分子质量=
≈3,即B分子中含有3个O原子,则有机物B的相对分子质量=![]() =138,A溶液具有酸性,1molA水解得到1molB和1mol醋酸,可知B中含有-COOH、-OH,B分子是去掉1个-COOH、-OH属于基团的式量=138-45-17=76,则属于基团中C原子最大数目为
=138,A溶液具有酸性,1molA水解得到1molB和1mol醋酸,可知B中含有-COOH、-OH,B分子是去掉1个-COOH、-OH属于基团的式量=138-45-17=76,则属于基团中C原子最大数目为![]() =6…4,故为-C6H4-,B的分子式为C7H6O3;根据B+CH3COOH→A+H2O可知A的分子式为C9H8O4。
=6…4,故为-C6H4-,B的分子式为C7H6O3;根据B+CH3COOH→A+H2O可知A的分子式为C9H8O4。
(1)根据B+CH3COOH→A+H2O可知,Mr(A)-Mr(B)=Mr(CH3COOH)-Mr(H2O)=60-18=42;
(2)根据以上分析可知B中含有3个氧原子;
(3)根据分析可知A的分子式为C9H8O4。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列五种有机物中:A.CH4;B.CH2=CH2;C.CH3CH2OH;D.CH3COOH;E.淀粉。
(1)C分子中含有的官能团的名称是_____;
(2)A分子的结构式是_____;
(3)水溶液显酸性的是_____(填编号);
(4)可用于合成聚乙烯塑料的是_____(填编号),化学反应方程式为_____________________ ;
(5)通常用于检验碘单质的是_____(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某石油化工产品X的转化关系如图,下列判断不正确的是( )
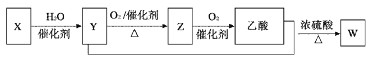
A. X可以发生加聚反应B. Y能与钠反应产生氢气
C. Z与CH3OCH3互为同分异构体D. W的结构简式为CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价电子排布式为3s23p4的粒子描述正确的是( )
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.它可与H2生成液态化合物
D.其电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾 (K2FeO4)是一种优良的水处理剂,将其溶于水中缓慢发生发应 4FeO42-+10H2O![]() 4Fe (OH)3+8OH -+3O2↑。在 pH=4.7 的溶液中,配成 c (K2FeO4)=1.0×10-3mol·L-1 试样,分别置于 20-60℃的恒 温水浴中,测定 K2FeO4 总量的变化如图,纵坐标为试样的浓度, 则下列说法不正确的是
4Fe (OH)3+8OH -+3O2↑。在 pH=4.7 的溶液中,配成 c (K2FeO4)=1.0×10-3mol·L-1 试样,分别置于 20-60℃的恒 温水浴中,测定 K2FeO4 总量的变化如图,纵坐标为试样的浓度, 则下列说法不正确的是
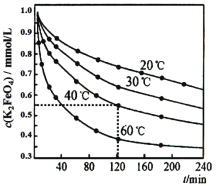
A.试样溶液的酸性越强,K2FeO4 越不稳定
B.40℃时,在 0~120 min 内,K2FeO4 的分解速率为3.75×10-3 mol·Lˉ1·minˉ1
C.由图可知,反应体系温度越高,分解速率越快
D.当分解足够长时间后,四份试样的分解率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化铬的化学式为 CrO5,从其结构发现含有 2 个过氧键,结构如图, 下列说法不正确的是

A.CrO5可能具有强氧化性
B.CrO5 溶于水可能放出氧气
C.CrO5 稳定性较低,易分解
D.CrO5 中 Cr 的化合价为+10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,其中浓硫酸除了做吸水剂和脱水剂的作用外还有_________;
[装置设计]甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是__(选填“甲”或“乙”).丙同学将甲装置中的玻璃管改成了球形干燥管除起冷凝作用外,它的另一重要作用是_________;
[实验步骤](1)按选择的装置组装仪器,在试管中先加入3mI乙醇,2m1冰醋酸,并在摇动下缓缓加入2mI浓硫酸充分摇匀,(2)将试管固定在铁架上;(3)在试管②中加入适量的饱和Na2CO3溶液;(4)用酒精灯对试管①加热;(5)当观察到试管②中有明显现象时停止实验。

[问题讨论]a.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:无色油状液体、____;
b.试管②中饱和Na2CO3的作用是溶解乙醇、降低乙酸乙酯的溶解度还有______的作用;
c.从试管②中分离出乙酸乙酯的实验操作是______;
d、生成乙酸乙酯的化学反应方程______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HCOOH和CH3COOH的电离常数分别1.80×104和1.75×105。将pH=3,体积均为V0的两种酸溶液分别加水稀释至体积V,pH随lg![]() 的变化如图所示。下列叙述错误的是( )
的变化如图所示。下列叙述错误的是( )
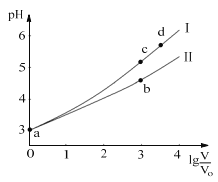
A.溶液中水的电离程度:b点<c点
B.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
C.从c点到d点,溶液中![]() 不变(HA、A-分别代表相应的酸和酸根离子)
不变(HA、A-分别代表相应的酸和酸根离子)
D.若两溶液无限稀释,则它们的c(H+)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以方铅矿(PbS)为原料制备铅蓄电池的电极材料的工艺流程如图所示: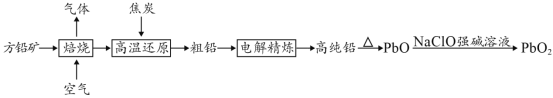
请回答下列问题:
(1)“焙烧”生成的气体直接排放可能造成的环境问题是____________,“焙烧”前须将方铅矿研磨粉粹的目的是________________________________。
(2)电解时,如c(Pb2+)远大于c(H+),则Pb2+优先于H+放电,工业上应用此原理可对铅进行电解精炼。“粗铅”的杂质主要有锌、铁、铜、银等,则阳极泥的主要成分为_________。
(3)写出制备PbO2的离子方程式________________________。
(4)已知部分含铅化合物的Ksp如下表所示:
物质 | PbCl2 | PbS |
Ksp | 1.2×10-5 | 9.0×10-29 |
①铅与稀盐酸反应产生少量气泡后反应终止,原因是_____________________。
②Pb(NO3)2是强酸弱碱盐,氢硫酸是弱酸[Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15],已知K>105时可以认为反应基本完全,通过计算判断向Pb(NO3)2溶液中通入H2S气体能否形成PbS沉淀___________________。(要求写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com