
用高铁酸钠(Na2FeO4)对河(湖)水消毒是城市饮水处理的新技术。已知反应
Fe2O3+3Na2O2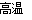 2Na2FeO4+Na2O,下列说法正确的是
2Na2FeO4+Na2O,下列说法正确的是
A.Na2O2既是氧化剂又是还原剂
B.3 mol Na2O2发生反应,有12 mol电子转移
C.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
D.Na2FeO4既是氧化产物又是还原产物
科目:高中化学 来源:2014高考名师推荐化学热化学方程式的正误判断及书写(解析版) 题型:选择题
已知:
①I2(g)+H2(g)  2HI(g) ΔH1=-9.48 kJ/mol
2HI(g) ΔH1=-9.48 kJ/mol
②I2(s)+H2(g)  2HI(g) ΔH2=+26.48 kJ/mol
2HI(g) ΔH2=+26.48 kJ/mol
下列判断正确的是
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.I2(g)===I2(s) ΔH=-17.00 kJ/mol
C.固态碘的稳定性比气态碘的稳定性高
D.1 mol固态碘和1 mol气态碘分别与氢气完全反应,前者断裂的I—I键更多
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氮气、氧化物及硝酸(解析版) 题型:选择题
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是
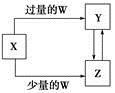
选项 | W | X |
A | 盐酸 | Na2CO3溶液 |
B | 稀HNO3 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | O2 | Na |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原规律(解析版) 题型:选择题
已知氧化性:Cl2>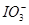 >Fe3+>I2,以下实验的结论或实验的预测合理的是
>Fe3+>I2,以下实验的结论或实验的预测合理的是
A.往溶液中加入过量的氯水再加淀粉,振荡不出现蓝色,说明没有I-
B.向FeCl2溶液中滴加碘水,所得溶液中加入KSCN溶液将呈红色
C.向淀粉碘化钾试纸上滴白醋和加碘盐的溶液,试纸变蓝,说明加碘盐中有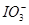
D.往FeI2溶液中滴加少量氯水,溶液变成棕黄色,说明有Fe3+生成
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原概念(解析版) 题型:选择题
铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:
(1)Tl3++2Ag=Tl++2Ag+
(2)Ag++Fe2+=Ag+Fe3+
(3)Fe+2Fe3+=3Fe2+,
下列离子氧化性比较顺序正确的是
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe2+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原反应方程式的配平及相关计算(解析版) 题型:填空题
已知:氧化性:KMnO4>HNO3;Bi位于周期表中ⅤA族,+3价较稳定,Bi2O3为碱性氧化物,Bi3+的溶液为无色。取一定量硝酸酸化的Mn(NO3)2溶液依次进行下列实验,现象记录如下:
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式: 。
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为 。
(3)向反应③得到的溶液中通入SO2气体,看到的现象是 。
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为 mol。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原反应方程式的配平及相关计算(解析版) 题型:选择题
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O;NO+NO2+2NaOH=2NaNO2+H2O。
则生成的盐溶液中NaNO2的物质的量为
A.0.4 mol B.0.6 mol
C.0.8 mol D.0.2 mol
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学气体制备(解析版) 题型:选择题
利用下列各组中的物质制备并收集相应的气体,能采用如图所示装置的是
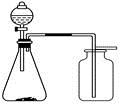
A.浓氨水和固体NaOH制NH3
B.过氧化氢溶液和二氧化锰制O2
C.稀硝酸和铜片制NO
D.电石和饱和食盐水制乙炔
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学探究组成、性质的实验方案的设计与评价(解析版) 题型:实验题
某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀。甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,他们设计实验测定沉淀中CuCO3的质量分数。
(1)按照甲同学的观点,发生反应的离子方程式为 。
(2)乙同学认为有Cu(OH)2生成的理论依据是 (用离子方程式表示)。
(3)两同学利用下图所示装置进行测定
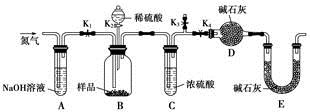
①在研究沉淀物组成前,须将沉淀从溶液中分离并净化。具体操作依次为 、洗涤、干燥。
②装置E中碱石灰的作用是 。
③实验过程中有以下操作步骤:
a.关闭K1、K3,打开K2、K4,充分反应
b.打开K1、K4,关闭K2、K3,通入过量空气
c.打开K1、K3,关闭K2、K4,通入过量空气
正确的顺序是 (填选项序号,下同)。
若未进行步骤 ,将使测量结果偏低。
④若沉淀样品的质量为m g,装置D的质量增加了n g,则沉淀中CuCO3的质量分数为 。
(4)丙同学认为还可以通过测量CO2的体积或测量 来测定沉淀中CuCO3的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com