
I.下列说法中正确的是 。
A.第一电离能由大到小的顺序为O>N>C
B.由于C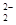 和O
和O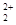 互为等电子体,所以可以推断O
互为等电子体,所以可以推断O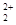 的电子式为
的电子式为
C.根据岩浆晶出规则,Ca0比Mg0更容易在岩浆冷却过程中先结晶
D.液态HF通常也可以写成(HF)n的形式,是因为液态HF分子间存在氢键
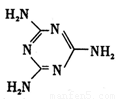
Ⅱ.(1)兰聚氰胺分子的结构简式如图所示,则其中氮原子轨道杂化类型是 ,l mol三聚氰胺分子中含 mol 键。
键。
(2)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的M层电子排布式为____ 。
(3)过渡金属配合物Ni( CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=____ 。
(4)碳化硅的晶胞结构(如右图)与金刚石类似(其中“●”为碳原子,“○”为硅原子)。图中“●”点构成的堆积方式与下列图式中 所表示的堆积方式相同。
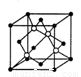

(5)碳化硅的结构中,与碳原子距离最近且相等的碳原子有 个。设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为 (用含a、b、c的式子表示)。
Ⅰ BD(3分)
Ⅱ (1)sp2、sp3 (2分) 15(1分)
(2)3s23p63d8(2分)
(3)4(2分)
(4)D(2分)
(5)12(1分) [2π(b3+c3)/3a3]×100%(2分)
【解析】I.A.不正确,第一电离能由大到小的顺序为N>O>C,N的2P能级是半充满结构,比较稳定;
B.正确,由于C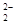 和O
和O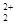 互为等电子体,结构相似;
互为等电子体,结构相似;
C.不正确,根据岩浆晶出规则:晶体从岩浆析晶难易程度不仅与岩浆的组成有关而且也与析出晶体的晶格能大小有关:晶格能高的晶体熔点较高更容易在岩浆冷却过程中先结晶,Mg0比Ca0更容易在岩浆冷却过程中先结晶。
D.正确,液态HF通常也可以写成(HF)n的形式,F原子电负性大,液态HF分子间存在氢键。
答案:B D
Ⅱ⑴六元环上的N是sp2杂化,氨基上的N是sp3杂化;l mol三聚氰胺分子中含 (6+3×3)mol=15mol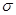 键,答案:sp2杂化、sp3杂化,15mol。
键,答案:sp2杂化、sp3杂化,15mol。
⑵第四周期VIII族有Fe、CO、Ni三种原子,基态碳原子的未成对电子数是2,三种原子中基态未成对电子数是2的是Ni,基态原子的M层电子排布式为3S23P63d8,答案:3S23P63d8
⑶Ni:3d8 4s2 为10e,CO:2e,10e + 2e×n = 18,n = 4,CO中只有C提供孤对电子,而C只有一对孤电子对;答案:4;
⑷碳原子构成的堆积方式与D相同,答案:D。
⑸碳化硅的结构中,与碳原子距离最近且相等的碳原子有12个;该晶胞中C为8×1/8+6×1/2=4,Si原子是4个,球体积公式为V=4/3πR3,原子体积=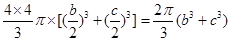 ,空间的利用率为
,空间的利用率为
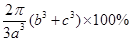 ,答案:12,
,答案:12,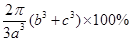 。
。
考点:物质的结构,核外电子排布,分子结构、晶体结构、空间利用率计算


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:同步题 题型:不定项选择题
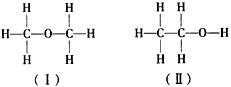
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com