
【题目】在一定温度下,恒容密闭容器中,发生反应:X(g)+Y(g)![]() Z(g)
Z(g) ![]() ,各物质的浓度随时间变化如图所示。
,各物质的浓度随时间变化如图所示。
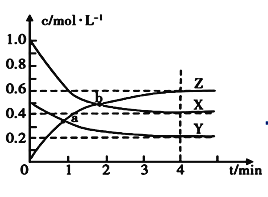
(1)从反应开始到4min时平衡,X的平均反应速率为________________。
(2)根据图像数据,4min时平衡常数K=________________。
(3)若使平衡时体系中c(X)=c(Z),则改变条件为 ________________。(只写一项)
(4)若某时刻,v正(Y)=2v逆(Z),则反应___________达平衡(填“已”或“未”)
(5)图中a.b对应的正反应速率大小关系为va_____vb(填“大于”、“等于”或“小于”)
【答案】0.15mol/(L.min)11.25适当升高温度、减小压强、加入X、减少Z或Y未大于
【解析】
(1)从反应开始到4min时平衡,X的平均反应速率为v=![]() ;(2)根据图像数据,4min时X、Y、Z改变的浓度分别为0.6mol/L.、0.3mol/L、0.6mol/L,根据化学反应速率之比等于化学计量数之比,可知反应为2X(g)+Y(g)
;(2)根据图像数据,4min时X、Y、Z改变的浓度分别为0.6mol/L.、0.3mol/L、0.6mol/L,根据化学反应速率之比等于化学计量数之比,可知反应为2X(g)+Y(g)![]() 2Z(g)。达平衡时的浓度分别为0.4mol/L.、0.2mol/L、0.6mol/L,故平衡常数K=
2Z(g)。达平衡时的浓度分别为0.4mol/L.、0.2mol/L、0.6mol/L,故平衡常数K=![]() ;(3)若使平衡时体系中c(X)=c(Z),则使平衡逆向移动增大X的浓度减小Z的浓度,反应2X(g)+Y(g)
;(3)若使平衡时体系中c(X)=c(Z),则使平衡逆向移动增大X的浓度减小Z的浓度,反应2X(g)+Y(g)![]() 2Z(g)
2Z(g) ![]() 为气体体积减小的放热反应,故改变条件可为适当升高温度、减小压强、加入X、减少Z或Y;(4)若某时刻,v正(Y)=2v逆(Z),根据反应的计量数可知,正反应速率大于逆反应速率,则反应未达平衡;(5)根据浓度越大反应速率越快,图中a.b对应Z的浓度在减小,则对应的正反应速率大小关系为va大于vb。
为气体体积减小的放热反应,故改变条件可为适当升高温度、减小压强、加入X、减少Z或Y;(4)若某时刻,v正(Y)=2v逆(Z),根据反应的计量数可知,正反应速率大于逆反应速率,则反应未达平衡;(5)根据浓度越大反应速率越快,图中a.b对应Z的浓度在减小,则对应的正反应速率大小关系为va大于vb。


科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是
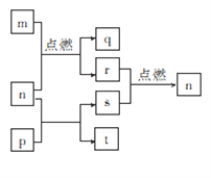
A. 原子半径:Z>Y
B. 化合物p中只存在离子键
C. 最简单气态氢化物的稳定性:W>X
D. 图示转化关系涉及的反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是2SO3(g)![]() 2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
2SO2(g)+O2(g)的能量变化图,据图得出的相关叙述正确的是( )
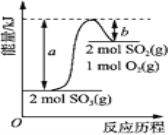
A. 该化学反应过程中既有能量的吸收又有能量的释放
B. 2SO3(g)![]() 2SO2(g)+O2(g) △H=-(a-b) kJ/mol
2SO2(g)+O2(g) △H=-(a-b) kJ/mol
C. 1 mol SO2的能量比1 mol SO3的能量高
D. 若某容器内有2 mol SO3充分反应,吸收(a-b) kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种常见的有机物,其中A的产量通常用来衡量一个国家的石油化工发展水平,B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省略):
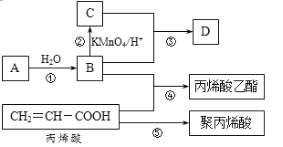
(1)B的结构简式为______________,C中官能团的名称为__________。
(2)丙烯酸(CH2=CH-COOH)的性质可能有_______________。(多选)
A.加成反应 B.取代反应 C.中和反应 D.氧化反应
(3)用一种方法鉴别B和C,所用试剂是___________________。
(4)丙烯酸乙酯的结构简式为_______________。
(5)写出下列反应方程式和有机反应基本类型:
③___________________________,___________反应;
⑤___________________________,___________ 反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是
A.FeO、Fe2O3、Na2O2均为碱性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.盐酸、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是
A. 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-===3Fe3++NO↑+2H2O
B. 铜片与浓HNO3:Cu+NO3-+4H+===Cu2++NO↑+2H2O
C. 氯化铵浓溶液跟浓NaOH溶液混合后加热:NH4++OH-![]() NH3·H2O
NH3·H2O
D. 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是
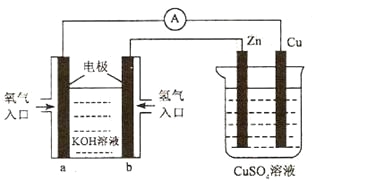
A. 该装置中Cu极为正极
B. 当铜极的质量变化为12 .8g时,a极上消耗的O2在标准状况下的体积为2.24L
C. b极反应的电极反应式为:H2-2e-=2H+
D. 一段时间后锌片质量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图![]() X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该融雪剂的化学式为________。
(2)Z、W元素的名称为________、_______。
(3)下列说法正确的是________。
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。
A.XY2的电子式:![]()
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-=2Y+Z↓
D.用电子式表示XY2的形成过程为:![]()
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】寻求和制备代号称“黑金”的新能源已经成为紧迫任务,化学工作者正在研究以天然气和醇类合成优质汽油的方法。已知:
⑴凡与醛基直接相连的碳原子上的氢称为α-H原子,在稀碱溶液的催化作用下,一个醛分子上的α-H原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:
R-CH2-CHO+R1-CH2-CHO![]() R-CH2-
R-CH2-![]() -
-![]()
⑵ 2R-CH2-Cl+2Na![]() R-CH2-CH2-R+2NaCl
R-CH2-CH2-R+2NaCl
⑶ CH3-CH=CH2+H-Cl![]() CH3-
CH3-![]() -CH3
-CH3
合成路线如下:
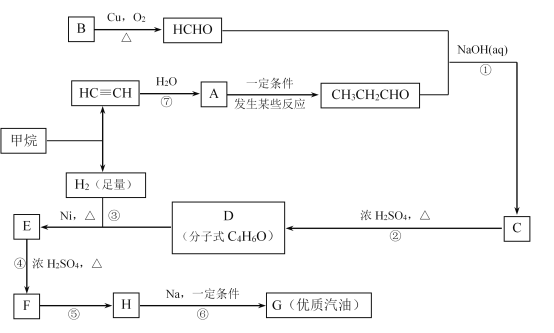
(1)在反应②~⑦中,属于加成反应的是____________,属于消去反应的是____________。
(2)写出下列反应方程式:
E → F:____________________________________________________;
H → G:___________________________________________________。
(3)H也能与NaOH溶液反应,其反应方程式为______________________________,生成的有机物能否在Cu或Ag作催化剂的条件下被空气氧化_______(选填“能”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com