
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c0(X)、c0(Y)、c0(Z)(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c0(X)、c0(Y)、c0(Z)(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c0(X)∶c0(Y)=3∶1
B. 平衡时,Y和Z的生成速率之比为2∶3
C. X、Y的转化率不相等
D. c0(X)的取值范围为0 mol·L-1<c0(X)<0.14 mol·L-1
【答案】D
【解析】
A项,可根据反应转化关系和平衡浓度计算初始浓度关系;B项,达到平衡状态时,正逆反应速率相等;C项,起始量相同,平衡量相同,转化率相同;D项,根据可逆反应不能完全转化,利用极值转化法分析。
列出“三段式”浓度:
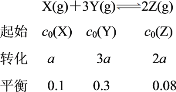
A项,c0(X)∶c0(Y)=(a+0.1)∶(3a+0.3)=1∶3,故A错误;B项,平衡时,正逆反应速率相等,v逆(Y)∶v正(Z)=3∶2,故B错误;C项,X、Y的转化率之比为:![]() ∶
∶![]() =1∶1,故C错误;D项,反应为可逆反应,物质不可能完全转化,如反应向逆反应方向进行,则c0(X)>0,如反应向正反应方向进行,则c0(X)<0.14molL-1,所以0<c0(X)<0.14molL-1,故D正确。综上所述,符合题意的选项为D。
=1∶1,故C错误;D项,反应为可逆反应,物质不可能完全转化,如反应向逆反应方向进行,则c0(X)>0,如反应向正反应方向进行,则c0(X)<0.14molL-1,所以0<c0(X)<0.14molL-1,故D正确。综上所述,符合题意的选项为D。


科目:高中化学 来源: 题型:
【题目】A原子的质量为ag,12C原子的质量为bg,NA为阿伏加德罗常数,下列说法正确的是( )
A. A元素的相对原子质量为12a/bB. mgA原子的物质的量为(m/aNA)mol
C. 该原子的摩尔质量为aNAgD. ng该A原子所含的中子数与质子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有的同学根据组成或性质将Na2CO3、NaOH、NaCl划分为一类。下列选项中的物质根据分类依据(后者是分类依据)能与上述三种物质归为一类的是
A.NaNO3(都属于钠盐)B.CuSO4(都易溶于水)
C.KNO3(都能与AgNO3溶液反应)D.KMnO4(固态时均为白色)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料,某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
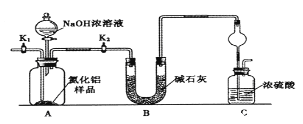
(1)如图C装置中球形干燥管的作用是______________。
(2)完成以下实验步骤:组装好实验装置,首先______;再加入实验药品。接下来的实验操作是____,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是______________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见_________。
(方案2)用如下图装置测定m g样品中A1N的纯度(部分夹持装置已略去)。
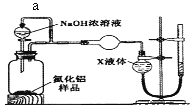
(4)导管a的主要作用是______________。
(5)为测定生成气体的体积,量气装置中的X液体可以是____________。(填选项序号)
a.CCl4 b.H2O c.NH4Cl溶液 d.![]()
(6)若mg样品完全反应,测得生成气体的体积为VmL,(已转换为标准状况),则A1N的质量分数为___(用含V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬合金有重要的用途,从其废料中制取铬的流程如下:
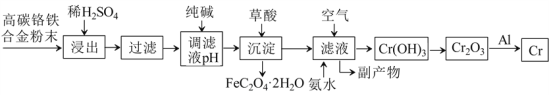
已知: ① Cr+H2SO4=CrSO4+H2↑,
② 流程中铬元素浸出之后至生成Cr(OH)3之间均以自由移动离子状态存在于溶液中。
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有:________________________ (写一条即可) 。
(2)用纯碱调节滤液pH,得到某弱碱沉淀,若纯碱过量,则可能导致的后果是_:_____________。
(3)流程中的“副产物”中,可用作可溶性钡盐中毒解毒剂的物质的化学式是___________;可用作化肥的物质的化学式是_____________。
(4)加入草酸实现沉淀转化反应化学方程式为:_______________________________________。
(5)流程中利用铝热反应冶炼铬的化学方程式为:_____________________________________。
(6)流程中由滤液生成Cr(OH)3的化学方程式为:_____________________________________。
(7)除已知反应①之外,整个流程中涉及的主要氧化还原反应有_____个,分解反应有____个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 200 mL 2 mol·L-1的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2===4Fe3++3Br2+10Cl-
B. 以石墨作电极电解氯化铝溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C. 氢氧化钠溶液吸收足量SO2气体:SO2+2OH-===SO![]() +H2O
+H2O
D. 向明矾溶液中加入氢氧化钡溶液至沉淀的物质的量最大:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com