
| A. | 100mL容量瓶 | B. | 分液漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
分析 配制一定物质的量浓度溶液实验操作的步骤:计算、称量、溶解、恢复室温、移液、洗涤、定容、摇匀等,依据各步用到的仪器解答.
解答 解:配制一定物质的量浓度溶液实验操作的步骤有计算、称量、溶解、恢复室温、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,并用玻璃棒搅拌,恢复室温后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯和玻璃棒2~3次,并将洗涤液移入容量瓶中,继续当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加水到凹液面与刻度线水平相切,盖好瓶塞,反复颠倒上下摇匀,移入试剂瓶贴标签贮存,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管等,用不到分液漏斗,
故选:B.
点评 本题考查一定物质的量浓度溶液的配制,比较基础,根据实验操作的步骤确定需要的仪器,进而判断不需要的仪器,题目难度不大,侧重考查学生基础实验能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
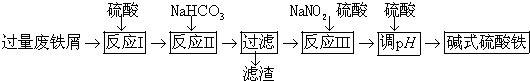
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应达到限度时,正逆反应速率相等 | |
| D. | 化学反应进行的时间越长该反应的限度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
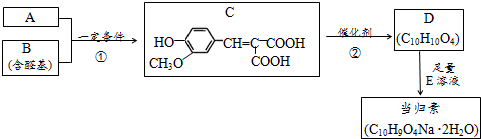
 ;
;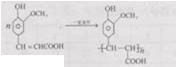 ;
;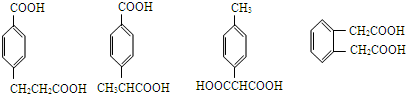 (其中两种).
(其中两种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数由多到少的顺序:Z>Y>W>X | |
| B. | X、Y、Z三种元素形成的化合物中只有共价键 | |
| C. | 简单气态氢化物的热稳定性:Y>Z | |
| D. | 最高价氧化物对应水化物的酸性:W>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
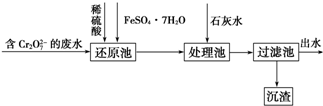
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
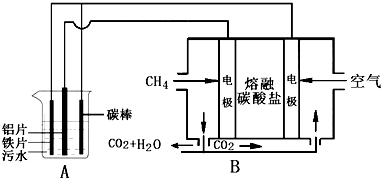
| A. | 装置B中通CH4一极电极反应为:CH4+4CO32--8e-═5CO2+2H2O | |
| B. | 装置B中CO32-向CH4一极移动 | |
| C. | A中阳极相关反应有:Fe-2e-═Fe2+ 2H2O-4e-═4H++O2↑ 12Fe2++3O2+6H2O═4Fe(OH)3↓+8Fe3+ | |
| D. | 标准状况下,若A装置中产生44.8 L气体,则理论上B装置中要消耗CH411.2L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com