
| A. | 被氧化的HCl为1.4mol | B. | 转移电子1.806×1023 | ||
| C. | 氧化产物为0.2mol | D. | 还原剂占参加反应HCl的$\frac{3}{7}$ |
分析 K2Cr2O7+HCl→KCl+CrCl3+Cl2↑+H2O反应中,氯元素失电子化合价由-1价升高到0价,Cr元素从+6价降低到+3价,则配平好的方程式为:K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,1molK2Cr2O7参加反应时,消耗14molHCl其中只有6mol被氧化,据此分析.
解答 解:A.1molK2Cr2O7参加反应时,消耗14molHCl其中只有6mol被氧化,则0.1molK2Cr2O7参加反应时,被氧化的HCl为0.6mol,故A错误;
B.0.1molK2Cr2O7参加反应时,被氧化的HCl为0.6mol,转移电子数0.6×6.02×1023=3.612×1023,故B错误;
C.0.1molK2Cr2O7参加反应时,被氧化的HCl为0.6mol,生成氧化产物为0.3molCl2,故C错误;
D.1molK2Cr2O7参加反应时,消耗14molHCl其中只有6mol被氧化,则还原剂占参加反应HCl的$\frac{3}{7}$,故D正确.
故选D.
点评 本题考查了氧化还原反应,注意根据元素化合价变化分析解答,侧重于考查学生的分析能力,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KHSO4 | B. | Fe2(SO4)3 | C. | KOH | D. | HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2、Cl2、SO2使品红溶液褪色原理不同 | |
| B. | Na2O2和SO2反应时,过氧化钠既作氧化剂又作还原剂 | |
| C. | 为了褪色更快,可同时向品红溶液通入等物质的量Cl2和SO2 | |
| D. | 可用H2S溶液来区别Cl2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
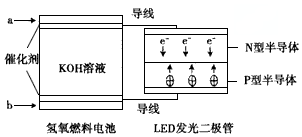
| A. | 电池负极电极反应式为H2-2e-+2OH-=2H2O | |
| B. | a处通入氧气,b处通入氢气 | |
| C. | 该装置中能量转化只涉及两种形式的能量 | |
| D. | P一型半导体连接的是电池负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可将地下输油钢管与外加直流电源的负极相连以保护钢管不受腐蚀 | |
| B. | 常温条件下,铝在空气中不易被腐蚀 | |
| C. | 镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更耐腐蚀 | |
| D. | 用锌与稀硫酸刮氢气时,往稀硫酸中滴少量硫酸铜溶液能加快反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com