
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 变成血红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6],振荡 | 产生蓝色沉淀 | 存在Fe2+ |
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
分析 (1)铁离子与硫氰酸钾溶液反应生成血红色溶液验证铁离子的存在;亚铁离子的检验是K3[Fe(CN)6]溶液和亚铁离子结合生成蓝色沉淀,据此进行解答;
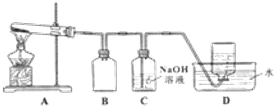
(2)装置中B为安全瓶,能够防倒吸;
(3)根据实验室中常用的检验氧气的方法解答;
(4)实验操作加入的试剂若是硝酸,固体溶解,银单质反应溶解,氧化银也能溶于硝酸;
装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,依据实验a可知产物为银,氧化银溶于氨水.
解答 解:(1)取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡,若含有铁离子溶液会变血红色,验证亚铁离子实验是取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6]溶液会和亚铁离子反应生成蓝色沉淀,
故答案为:溶液呈血红色;K3[Fe(CN)6]溶液;产生蓝色沉淀;
(2)装置导气管略露出胶塞,是安全瓶,可以防止C装置中的液体到吸入发生装置A,
故答案为:防倒吸;
(3)氧气具有助燃性,用带火星的木条伸入集气瓶中,木条复燃证明无色气为氧气,
故答案为:用带火星木条靠近瓶口,木条复燃,证明是氧气;
(4)b实验加入的硝酸可以溶解Ag2O,也可以溶解Ag,不能检验固体成分,
实验a加入氨水,银不能溶解于氨水溶液,Ag2O能溶于氨水中形成银氨溶液,可以验证固体成分的判断,加入足量氨水,振荡黑色固体不溶解,说明生成的固体为Ag,装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,AgNO3固体热分解的产物有Ag、NO2、O2,
故答案为:b;Ag、NO2、O2.
点评 本题为探究实验题,考查实验操作、装置的作用、物质的检验等知识,题目难度中等,注意掌握实验设计的方法和物质实验验证方案分析方法,侧重考查了学生提出假设并设计实验验证的能力、分析问题解决问题的能力及提取信息的能力.


科目:高中化学 来源: 题型:多选题
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 | |
| C. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
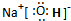 ,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
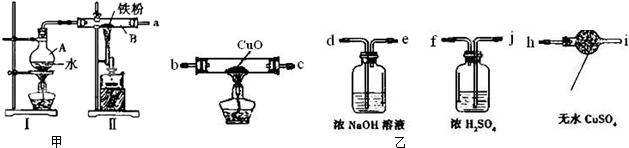
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
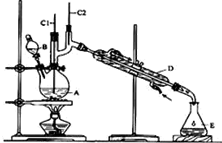 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO| 沸点/℃ | 密度(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子结构示意图 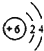 ,可以表示12C原子或13C原子 ,可以表示12C原子或13C原子 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 次氯酸的电子式 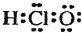 | |
| D. | CO2的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 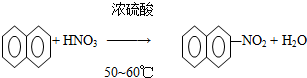 | |
| B. | 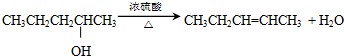 | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | (CH3)2CHCH=CH2+HI→(CH3)2CHCHICH3+(CH3)2CHCH2CH2 I |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com