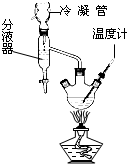
����ѧ�У�ͨ�������ط����о�����������ʱ�������仯��ȷ������ɣ�ȡ66.6mg�ɸ���ʯ[Al
4Si
4O
10��OH��
8]�ͷ���ʯ��CaCO
3����ɵĿ�����ȵ�673K��1123K�����ڷֽ�Ϊ�������Ʒ��ʧ��13.8mg������ʯ���ȷֽⷴӦ����ʽ��Al
4Si
4O
10��OH��
8��2Al
2O
3+4SiO
2+4H
2O
��1����ԭ�Ӻ�������Ų���
����ͬ�ĵ��Ӳ��У������������ӷֲ���
����ͬ�Ĺ���У�
��2��������ͬ���������ڣ���ѧ�����������ԣ�д��Si��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ
��
��3������ʯ�dz�ʯ��һ�֣���ͬ�ʯ����ԭ�ӵ����ʵ���������ͬ���ɸƳ�ʯ��ѧʽCaAl
2Si
2O
8����֪�Ƴ�ʯ�Ļ�ѧʽΪ
��
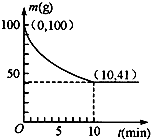
��4���˿����и���ʯ����������Ϊ
��
a��44% b��56% c��77.5% d��80%
��5�����Ը������������ջ��Ȼ������������зֽ⣬���ڷֽ�����Ȼ�����Һ�����������ٷֱ�������Һ����ȥ���ᴿ�����õ����Ȼ�����Һ���Ʊ���������д�����Ȼ�����Һ�õ������������Ļ�ѧ��Ӧ����ʽ��Ҫ�����Լ����
��
��6���ý�̿��ʯӢɰ��SiO
2����ϸ��£������ֹ裬�������ַ������ֹ��ᴿ��
��һ�ַ�����Si+2Cl
2 SiCl
4 SiCl
4+2H
2Si+4HCl
�ڶ��ַ�����Si+3HCl
SiHCl
3 SiHCl
3+H
2Si+3HCl��
��ҵ�ϳ��õڶ��ַ������ᴿ�����裬��ԭ����
��



 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
 �����������������ͻ�ѧ���ԣ��Ǹ�����ҵ����Ҫԭ�ϣ��ʻ����ᴿ�����漰��������Ӧ����Ϊ��
�����������������ͻ�ѧ���ԣ��Ǹ�����ҵ����Ҫԭ�ϣ��ʻ����ᴿ�����漰��������Ӧ����Ϊ��