
 ;
;
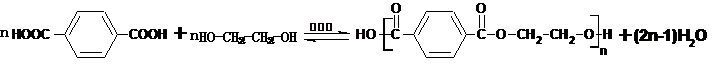
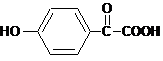 .
. .
.
 .
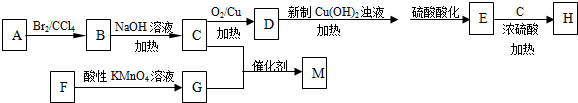
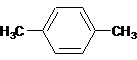
. 分析 A的产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与溴发生加成反应生成B为HBrCH2CH2Br,B发生水解反应反应生成C为HOCH2CH2OH,C发生催化氧化生成D为OHC-CHO,D发生氧化反应、酸化得到E为HOOC-COOH,H分子结构中含有六元环,则H为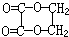 .烃F相对分子质量为106,则分子中最大碳原子数为$\frac{106}{12}$=8…10,其分子式为C8H10,F可以使酸性高锰酸钾溶液褪色,但不能使溴的CCl4溶液褪色,属于苯的同系物,核磁共振氢谱显示F分子结构中只有两种化学环境的氢,则F为
.烃F相对分子质量为106,则分子中最大碳原子数为$\frac{106}{12}$=8…10,其分子式为C8H10,F可以使酸性高锰酸钾溶液褪色,但不能使溴的CCl4溶液褪色,属于苯的同系物,核磁共振氢谱显示F分子结构中只有两种化学环境的氢,则F为
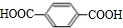 ,G与乙二醇发生缩聚反应生成M为
,G与乙二醇发生缩聚反应生成M为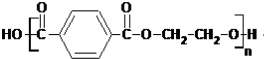 .
.
解答 解:A的产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与溴发生加成反应生成B为HBrCH2CH2Br,B发生水解反应反应生成C为HOCH2CH2OH,C发生催化氧化生成D为OHC-CHO,D发生氧化反应、酸化得到E为HOOC-COOH,H分子结构中含有六元环,则H为 .烃F相对分子质量为106,则分子中最大碳原子数为$\frac{106}{12}$=8…10,其分子式为C8H10,F可以使酸性高锰酸钾溶液褪色,但不能使溴的CCl4溶液褪色,属于苯的同系物,核磁共振氢谱显示F分子结构中只有两种化学环境的氢,则F为
.烃F相对分子质量为106,则分子中最大碳原子数为$\frac{106}{12}$=8…10,其分子式为C8H10,F可以使酸性高锰酸钾溶液褪色,但不能使溴的CCl4溶液褪色,属于苯的同系物,核磁共振氢谱显示F分子结构中只有两种化学环境的氢,则F为
 ,G与乙二醇发生缩聚反应生成M为
,G与乙二醇发生缩聚反应生成M为 .
.
(1)由C生成D的化学方程式为:HOCH2CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O,属于氧化反应,
故答案为:HOCH2CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O;氧化反应;
(2)H为 ,化学名称是乙二酸乙二酯,由C、G生成M的化学方程式:
,化学名称是乙二酸乙二酯,由C、G生成M的化学方程式: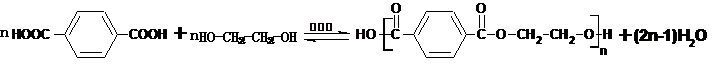
故答案为: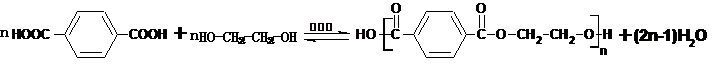
(3)F的结构简式为
故答案为:
(4)同时满足下列条件G( )的同分异构体:
)的同分异构体:
①能与Na2CO3溶液反应生成无色无味气体,说明含有羧基,②遇FeCl3溶液发生显色反应,说明含有酚羟基,可以含有2个取代基为-OH、-COCOOH,有邻、间、对3种,可以含有3个取代基为-OH、-CHO、-COOH,而-OH、-CHO有邻、间、对3种位置,对应的-COOH分别有4种、4种、2种,共有13种,其中核磁共振氢谱中有4组峰,且面积比为1:2:2:1的结构简式是: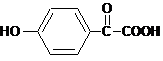
故答案为:13;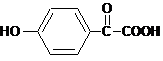
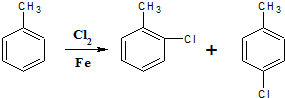
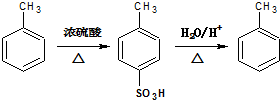
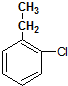
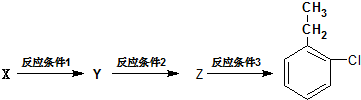
(5)X为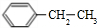 ,结合信息可知,乙苯与浓硫酸在加热条件下反应生成Y为
,结合信息可知,乙苯与浓硫酸在加热条件下反应生成Y为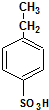 ,然后与氯气在Fe作催化剂条件下反应生成Z为
,然后与氯气在Fe作催化剂条件下反应生成Z为 ,最后再酸性条件下水解得到
,最后再酸性条件下水解得到 ,
,
故答案为:浓硫酸; Cl2/Fe; .
.
点评 本题考查有机物的推断与合成,注意根据反应条件进行推断,熟练掌握官能团的性质与转化,掌握相对分子质量确定烃的分子式,较好地考查学生自学能力、知识迁移运用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
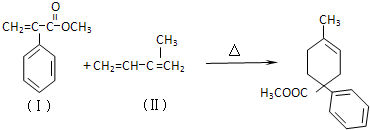
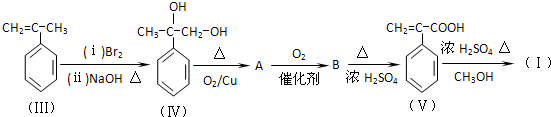
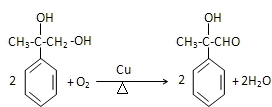 .
.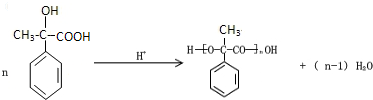 .
.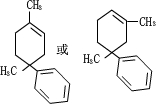 (任写一种)
(任写一种)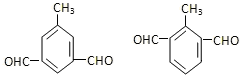 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
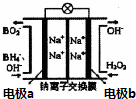 以NaBH4和H2O2为燃料的燃料电池可用于通信卫星.其负极材料采用Pt/C,正极材料采用MnO2,电池的工作原理如图所示.下列说法错误的是( )
以NaBH4和H2O2为燃料的燃料电池可用于通信卫星.其负极材料采用Pt/C,正极材料采用MnO2,电池的工作原理如图所示.下列说法错误的是( )| A. | 电池放电时,Na+从a极区移向b极区 | |
| B. | 电极b采用MnO2,该极附近溶液的pH保持不变 | |
| C. | 该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O | |
| D. | 电池放电时,电子从a极经导线流向b极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体B2C3不能从溶液中制得 | |
| B. | C的氧化物对应水化物为强酸 | |
| C. | B的简单离子半径大于D的简单离子半径 | |
| D. | AD2分子中各原子最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 倭铅是指金属锌和铅的混合物 | |
| B. | 煤炭中起作用的主要成分是C | |
| C. | 冶炼Zn的过程中有氧化还原反应发生 | |
| D. | 该冶炼锌的方法属于热还原法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3俗名纯碱,其水溶液显弱碱性 | |
| B. | 该溶液中K+、Al3+、SO42-可以大量共存 | |
| C. | 加水稀释该溶液,溶液中$\frac{c(HC{{O}_{3}}^{-})}{c(C{{O}_{3}}^{2-})}$增大 | |
| D. | 向该溶液中加入足量的氢氧化钙溶液的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
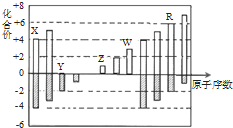
| A. | 原子半径:Z>Y>X | |
| B. | Z和Y形成的化合物是离子化合物 | |
| C. | 气态氢化物的稳定性:Y<R | |
| D. | 常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{10}$O | |
| B. | 氯离子的结构示意图: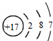 | |
| C. | 对苯二甲酸的结构简式: | |
| D. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
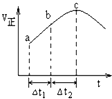 向某恒容密闭容器中通入N2和H2,在500℃时,使反应:N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向某恒容密闭容器中通入N2和H2,在500℃时,使反应:N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )| A. | 反应在c点达到平衡状态 | |
| B. | △t1=△t2时,N2的转化量:a~b段小于b~c段 | |
| C. | C点反应放出的热量达到最大 | |
| D. | 反应物浓度:a点小于b点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com