
已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O= 4Fe(OH)3↓+O2↑+8Na+ 则下列说法正确的是( )
A、该反应中 Fe2+是还原剂,O2 是还原产物
B、4molNa2O2 在反应中共得到 8NA 的电子
C、Fe(OH)3 既是氧化产物又是还原产物,每生成 4mol Fe(OH)3 反应过程中共转移电子 6mol
D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
关于醇和酚的叙述中正确的是( )
A.含有羟基官能团的有机物一定是醇
B.苯酚具有弱酸性,它的水溶液可使石蕊试液变红色
C.不慎将苯酚沾皮肤上,可用乙醇洗涤
D.醇的通式是CnH2n+1OH
查看答案和解析>>
科目:高中化学 来源: 题型:
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用煤矸石的工艺流程如下图所示。
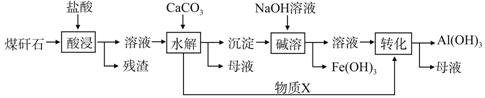
(1)写出“酸浸”过程中主要反应的离子方程式(任写一个):
。
(2)物质X的化学式为________。“碱溶”时反应的离子方程式为__________________。
(3)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得Al(OH)3产品,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续的操作过程是 ,再加入CaCO3调节pH到5.4,过滤得到Al(OH)3
(4)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3饱和溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体。结合化学平衡移动原理解释析出晶体的原因:
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Fe及其化合物的部分转化关系如图所示。下列说法不正确的是
A.①中硫酸的浓度可以为98% B.②中试剂可以是氨水或NaOH溶液
C.③中操作为蒸发浓缩、冷却结晶 D.X一定含有SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度低于570℃时反应的化学方程式 。
(2)中学教材中用右图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是
。
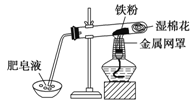
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图发生该反应并有氢气的收集装置图(包括反应时容器中的物质)。
 |
说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽:
 试管:
试管:
 蒸发皿:
蒸发皿:
 玻璃导管:
玻璃导管:
 或
或
 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)乙同学为了探究实验后的固体产物是否存在Fe3O4(假定铁全部反应完全)设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液X中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2符合 关系时,才能确定固体样品中一定只存在Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液可能含有Cl-、SO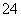 、CO
、CO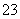 、NH
、NH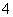 、Fe3+、Al3+和K+。取该溶液 100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、Fe3+、Al3+和K+。取该溶液 100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
A、至少存在5种离子 B、Cl-一定存在,且c(Cl-)≥0.4 mol·L-1
C、SO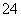 、NH
、NH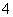 一定存在,Cl-可能不存在 D、CO
一定存在,Cl-可能不存在 D、CO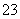 、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
根据陈述的知识,类推得出的结论正确的是
A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O
B. Fe与S直接化合生成FeS,则Cu与S直接化合生成Cu2S
C.少量CO2通入Ca(ClO)2溶液生成CaCO3,则少量SO2通入Ca(ClO)2溶液生成CaSO3
D. 已知第四主族沸点CH4<SiH4<GeH4,则第六主族沸点H2O<H2S<H2Se
查看答案和解析>>
科目:高中化学 来源: 题型:
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是 ( )
A.Th元素的质量数是232
B.Th元素的相对原子质量是231
C.232Th转化成233U是化学变化
D.230Th和232Th的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,对pH=10的氨水而言,下列说法正确的是( )
|
| A. | 溶液中由水电离的氢离子浓度为10﹣4 |
|
| B. | 与pH=4的盐酸等体积混合后,c(Cl﹣)>c(NH4+) |
|
| C. | 通入一定量氨气后,依然存在c(NH4+)+c(H+)=c(OH﹣) |
|
| D. | 氨水中存在:c(NH3•H2O)>c(NH4+)>c(OH﹣)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com