
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的.周期数与主族序数相等。
![]()
请回答下列问题:
(1)W在周期表中的位置是_________________________________,Q、R、T三种元素原子半径由大到小的顺序为________________________。(用元素符号表示),QO2的电子式为___________,比较Q、R的最高价氧化物的水化物的酸性__________________。(填物质的化学式)。
(2)T单质与NaOH 溶液反应的离子方程式为__________________________________________ 。
【答案】第3周期第ⅥA族 Al>C>N ![]() HNO3>H2CO3 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
HNO3>H2CO3 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
【解析】
图中所示是短周期元素Q、R、T、W在元素周期表中的位置,因为T所处的周期序数与主族族序数相等,所以T是Al,Q是C,R是N,W是S,据此解答。
根据以上分析可知T为Al,Q是C,R是N,W是S,则
(1)W为S,S有3个电子层,最外层6个电子,故处于第三周期ⅥA族;电子层数越多,半径越大,同一周期原子序数越小,半径越大,故C、N、Al三种元素原子的半径从大到小排列顺序Al>C>N,QO2为二氧化碳,CO2中C与O形成两对共价键,故电子式为![]() ;非金属性越强,最高价含氧酸的酸性越强,氮元素非金属性强于碳元素,则酸性HNO3>H2CO3;
;非金属性越强,最高价含氧酸的酸性越强,氮元素非金属性强于碳元素,则酸性HNO3>H2CO3;
(2)T为Al,与氢氧化钠反应的离子方程式为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑。


科目:高中化学 来源: 题型:
【题目】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的电子排布式为______;价电子中成对电子数有____个。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是_________。
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3___H3PO4(填“>”或“<”),从结构的角度说明理由:__________________________。
(3)磷青铜中的锡、磷两元素电负性的大小为Sn___P(填“>”“<”或“=”)。
(4)某磷青铜晶胞结构如图所示。

①则其化学式为________。
②该晶体中距离Cu原子最近的Sn原子有______个,这些Sn原子所呈现的构型为_________。
③若晶体密度为8.82g·cm-3,最近的Cu原子核间距为____pm(用含NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1999年4月,比利时查出污染鸡的根源是生产鸡饲料的油脂被二恶英所污染,二恶英是两大芳香族化合物的总称。其中四氯代二苯并二恶英毒性最大,其结构简式为:
下列有关该化合物的说法中正确的是( )

A. 分子式为C12H8O2Cl4
B. 是一种可溶于水的气体
C. 是最危险的致癌物之一
D. 是一种多卤代烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体说法的正确组合是

①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】5﹣二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5﹣二甲氧基苯酚的部分物理性质见下表:
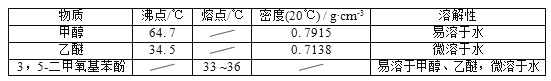
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取,①分离出甲醇的操作是的______;②萃取用到的分液漏斗使用前需__________________并洗净,分液时有机层在分液漏斗的________填(“上”或“下”)层;
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3溶液洗涤的目的是__,用饱和食盐水洗涤的目的是______;
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__(填字母);
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先________________,再______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:

(1)元素①可与18O组成多种水分子,其相对分子质量的最大值为_____;元素①可与元素②形成一种由五个原子构成的+1价阳离子,该离子所含电子数为____________;
(2)判断:已知元素④的非金属性比⑧强,故④的单质可以从⑧的可溶性盐溶液中置换出⑧的单质___。(填“正确”或“错误”)。
(3)元素⑤⑦的最高价氧化物的水化物发生反应的化学方程式为_________;
(4)为验证VIIA族部分元素非金属性的递变规律,设计了如图装置进行实验,请回答:
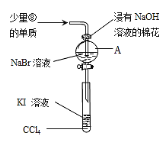
①A中发生的反应的离子方程式是_______;
②棉花中浸有的NaOH溶液的作用是_______;
③VIIA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下,____,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
![]()
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为______________________。
(3)沉淀B的化学式为___
II.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:

(4)毒重石用盐酸浸取前需充分研磨,目的是___________________________________。
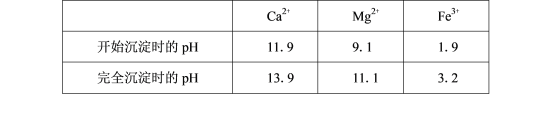
(5)滤渣Ⅱ中含________________(填化学式)。加入H2C2O4时应避免过量,原因是______________________。已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com