
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A. | 甲的金属性比乙强 | B. | 乙的化合价为+1价 | ||
| C. | 丙一定为非金属元素 | D. | 丁一定是金属元素 |
分析 甲、乙、丙、丁为第三周期元素,甲元素的第一电离能远远小于第二电离能,说明A元素最外层有1个电子,失去1个电子时达到稳定结构,所以甲为Na元素;乙元素的第二电离能远远小于第三电离能,则B元素最外层有2个电子,失去两个电子后达到稳定结构,所以乙为Mg元素;丙、丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层大于3个电子,丙、丁一定为非金属元素;结合结构和性质分析解答.
解答 解:甲、乙、丙、丁为第三周期元素,甲元素的第一电离能远远小于第二电离能,说明A元素最外层有1个电子,失去1个电子时达到稳定结构,所以甲为Na元素;乙元素的第二电离能远远小于第三电离能,则乙元素最外层有2个电子,失去两个电子后达到稳定结构,所以乙为Mg元素;丙、丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层大于3个电子,丙、丁一定为非金属元素.
A.甲为Na元素,乙为Mg元素,故甲的金属性比乙强,故A正确;
B.乙为Mg元素,化合价为+2价,故B错误;
C.丙元素最外层大于3个电子,丙、丁一定为非金属元素,故C正确;
D.丁一定为非金属元素,故D错误.
故选AC.
点评 本题考查了电离能与元素的金属性、非金属性的关系,第n电离能远远小于第(n+1)电离能时确定原子的最外层电子数,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
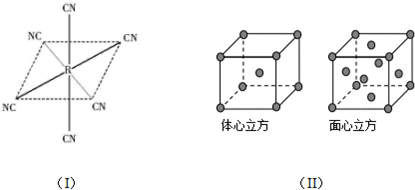
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 3:2 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+) 增大 | B. | Ka(HF)增大 | C. | $\frac{c({F}^{-})}{c({H}^{+})}$减小 | D. | $\frac{c({H}^{+})}{c(HF)}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气:K+、Na+、AlO2-、CO32- | B. | 二氧化硫:Na+、NH4+、SO32-、Cl- | ||
| C. | 氯化氢:H+、K+、MnO4-、SO42- | D. | 二氧化碳:Mg2+、Al3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂属于酯类,在酸性或碱性条件下与水发生水解反应,称为皂化反应 | |
| B. | 淀粉、纤维素没有甜味,它们都是天然高分子化合物,在一定条件下水解都能生成葡萄糖 | |
| C. | 鸡蛋清的溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质变性 | |
| D. | 氨基酸分子中都含有-COOH和-NH2二种原子团,能相互反应形成更复杂的多肽化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的还原产物是 I2 | |
| B. | 每生成 1 mol I2,转移的电子为 2 mol | |
| C. | KOH 和 O2 都是还原产物 | |
| D. | 反应中氧化剂与还原剂质量之比为 1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com