
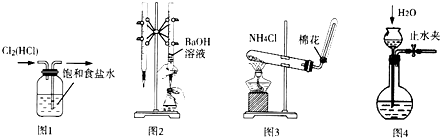
| A. | 用图l所示装置除去Cl2中的HCl杂质 | |
| B. | 用图2所示装置用标准浓度的氢氧化钠溶液测定盐酸的浓度 | |
| C. | 用图3所示装置实验室制取NH3 | |
| D. | 用图4所示装置检查装置气密性 |
分析 A.用饱和食盐水除去氯气中的HCl,且洗气装置中导气管应该采用“长进短出”原则;
B.盛放NaOH溶液的滴定管应该是碱式滴定管;
C.氯化铵受热分解生成氨气和氯化氢,氯化氢和氨气冷却立即生成氯化铵;
D.能产生压强差的装置能检验气密性.
解答 解:A.用饱和食盐水除去氯气中的HCl,且洗气装置中导气管应该采用“长进短出”原则,不符合实验要求,所以不能实现实验目的,故A错误;
B.盛放NaOH溶液的滴定管应该是碱式滴定管,该实验中滴定管为酸式滴定管,故B错误;
C.氯化铵受热分解生成氨气和氯化氢,氯化氢和氨气冷却立即生成氯化铵,应该用加热氯化铵和氢氧化钙混合物制取氨气,故C错误;
D.能产生压强差的装置能检验气密性,该装置能产生压强差,能检验装置气密性,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及气密性检验、气体制备、仪器选取、除杂等知识点,明确实验原理及物质性质、实验操作规范性是解本题关键,注意实验的评价性,题目难度不大.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F为前四周期元素,它们的原子序数依次增大.A、C的基态原子的电子排布中L能层都有两个未成对电子,C、D同主族,E的基态原子的电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.
A、B、C、D、E、F为前四周期元素,它们的原子序数依次增大.A、C的基态原子的电子排布中L能层都有两个未成对电子,C、D同主族,E的基态原子的电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满. .
. .DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.
.DAB-的水溶液可以用于实验室中E3+离子的定性检验,形成配合物的颜色为血红色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀锌铁的镀层破损后,镀层仍然对铁起保护作用 | |
| B. | 根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液 | |
| C. | Cl2与SO2使品红溶液褪色的原理相同 | |
| D. | SiO2可用于制造光导纤维,其性质稳定,不溶于强酸,但是能溶于强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下2.24L C12溶于水,发生反应转移的电子数一定为0.1NA | |
| B. | 1 mol的羟基(-OH)和l mol的OH-所含电子数均为1NA | |
| C. | 常温常压下,1.6gCH4中含有共价键总数为0.4NA | |
| D. | 室温下,1L 0.1mol•L-1CH3COONH4溶液中NH4+离子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
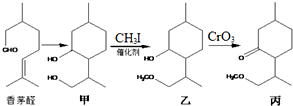
| A. | 香茅醛能发生加聚反应和缩聚反应 | |
| B. | “甲→乙”发生了取代反应 | |
| C. | 甲中不同化学环境的羟基化学性质不同 | |
| D. | 香茅醛存在顺反异构现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
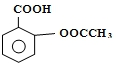 阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )
阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )| A. | 与乙酰水杨酸具有相同官能团的芳香族同分异构体共有8种(不考虑立体异构) | |
| B. | 乙酰水杨酸能发生取代、加成、氧化、还原反应 | |
| C. | 乙酰水杨酸的所有原子均在同一平面上 | |
| D. | 服用阿司匹林药量过大时,可出现精神错乱、惊厥甚至昏迷等水杨酸反应,可用硼酸溶液解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
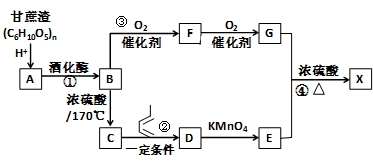

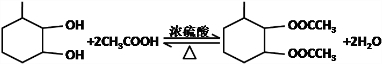 .
.
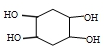 的合成路线为
的合成路线为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释 |
| A | 向AlCl3溶液中逐滴加入NaOH溶液并振荡 | 产生白色沉淀,后沉淀逐渐溶解 | 铝元素具有一定的非金属性 |
| B | 将Fe(NO3)2固体溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | 稀硫酸将Fe2+氧化为Fe3+ |
| C | 向KBrO3溶液中加入少量CCl4,然后通入少量Cl2,充分振荡,静置 | 下层呈橙色 | 氧化性:Cl2>Br2 |
| D | 将充有NO2的玻璃球放入热水中 | 红棕色加深 | 2NO2?N2O4△H>0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com