
【题目】25℃时,将0.0l mol L -1 NaOH溶液滴入20mL0.01mol·L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示。下列说法正确的是
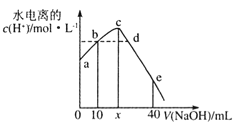
A. x=20,a点的纵坐标为1.0×10-12
B. b点和d点所示溶液的pH相等
C. 滴定过程中,c(CH3COO-)与c(OH-)的比值逐渐增大
D. e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、M、R为短周期元素,X、R在同一主族,![]() 与
与![]() 具有相同的电子层结构,X原子的L层电子数是K层电子数的2倍。判断下列说法正确的是
具有相同的电子层结构,X原子的L层电子数是K层电子数的2倍。判断下列说法正确的是
A.R的最高价氧化物对应水化物的酸性比Y的强
B.X、Y、M均可形成多种氧化物
C.X的简单气态氢化物的热稳定性比Y的强
D.离子半径的大小:r(![]() )>r(
)>r(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
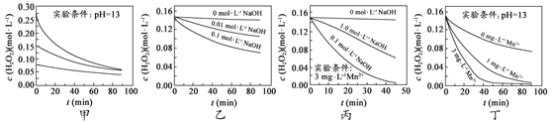
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据以下反应:
KMnO4+ Na2SO3+ H2SO4= MnSO4+ Na2SO4+ K2SO4+ H2O
回答下列问题:
I.请配平该反应方程式___,该反应还原剂是___,还原产物是___。
II.当反应转移1mol电子时,被氧化的物质的质量为___g。
Ⅲ.用单线桥法标出反应中电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?)△H>0,达到化学平衡后,进行下列操作。
3B(?)+C(?)△H>0,达到化学平衡后,进行下列操作。
(1)升高温度,用“变大”“变小”“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量______;
②若B、C都不是气体,气体的平均相对分子质量______;
③若B是气体,C不是气体,气体的平均相对分子质量______;
(2)如果平衡后温度保持不变,将容器体积增大一倍,新平衡时A的浓度是原来的50%,判断B的状态是__________态,C的状态是__________态。
(3)某密闭容器中放入一定量的NO2,发生反应2NO2![]() N2O4(正反应放热),达平衡后,若分别单独改变下列条件,重新达到平衡后,能使混和气体平均分子量增大的是_________。
N2O4(正反应放热),达平衡后,若分别单独改变下列条件,重新达到平衡后,能使混和气体平均分子量增大的是_________。
A.通入N2 B.通入NO2 C.通入N2O4 D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CO2和NH3为原料合成尿素。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)![]() NH2CO2NH4(s) ΔH1=-159.47 kJ·mol-1
NH2CO2NH4(s) ΔH1=-159.47 kJ·mol-1
反应Ⅱ:NH2CO2NH4(s) ![]() CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(g) ΔH3
CO(NH2)2(s)+H2O(g) ΔH3
回答下列问题:
(1)在相同条件下,反应Ⅰ分别在恒温恒容容器中和绝热恒容容器中进行,二者均达到平衡后,c(CO2)恒温________c(CO2)绝热(填“大于”“小于”或“等于”);ΔH3=____________。
(2)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4 mol NH3和0.2 mol CO2放入容积为2 L的密闭容器中,t1时达到化学平衡,c(CO2)随时间t变化曲线如图甲所示,在0~t1时间内该化学反应速率υ(NH3)=____________;若其他条件不变,t1时将容器体积压缩到1 L,t2时达到新的平衡。请在图甲中画出t1~t2时间内c(CO2)随时间t变化的曲线。___________________________________
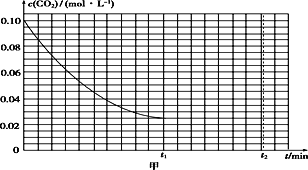
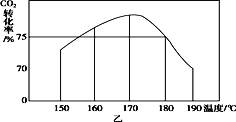
(3)在150 ℃时,将2 mol NH3和1 mol CO2置于a L 密闭容器中,发生反应Ⅲ,在t时刻,测得容器中CO2转化率约为73%,然后分别在温度为160 ℃、170 ℃、180 ℃、190 ℃时,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线(见图乙)。在150~170 ℃之间,CO2转化率呈现逐渐增大的变化趋势,其原因是__________180 ℃时反应Ⅲ的平衡常数K=____________(用含a的式子表示)。
(4)侯氏制碱法主要原料为NaCl、CO2和NH3,其主要副产品为NH4Cl,已知常温下,NH3·H2O的电离常数Kb=1.8×10-5,则0.2 mol·L-1 NH4Cl溶液的pH约为________(取近似整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是
反应②:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O;⑤为置换反应(反应条件已略去,漂白粉主要成分为Ca(ClO)2;)。

A.反应①②③④⑤均可写出离子方程式
B.相同条件下生成等量的O2,反应③和④转移的电子数之比为1: 1
C.反应①中氧化剂与还原剂的物质的量之比为1: 4
D.反应⑤说明该条件下铝的还原性强于锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空:
(1)同温同压下,同体积的甲烷和二氧化碳物质的量之比为____,质量比为____;
(2)在标准状况下,4 g H2,11.2 L O2,1 mol H2O中,所含分子数最多的是______,体积最小的是________;
(3)硫酸钾和硫酸铝的混合溶液中,已知其中Al3+的浓度为0.4 mol/L,SO42-的浓度为0.7 mol/L,则K+的浓度为________mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com