
| A、等体积,等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B、FeI2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| C、CH3COONH4的电离:CH3COONH4?NH4++CH3COO- |
| D、苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO32- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、原子半径大小:Z>Y>X>W |
| B、W、Y、Z中最简单氢化物稳定性最弱的是W |
| C、Z元素单质在化学反应中只表现氧化性 |
| D、z元素氧化物对应水化物的酸性一定强于Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
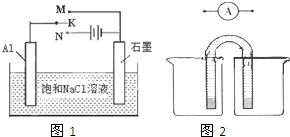 以下是一些物质的熔沸点数据(常压):
以下是一些物质的熔沸点数据(常压):| 钾 | 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 774 | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、若完全燃烧,1mol雄酮(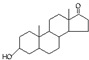 )比雌酮( )比雌酮( )多消耗3mol O2 )多消耗3mol O2 |
| B、正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 |
| C、蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 |
| D、乙醇依次通过消去、取代、加成反应可生成乙二醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁腐蚀时可能发生的正极反应:2H2O+O2+4e-═4OH- |
| B、明矾水解的离子方程式:Al3++3H2O?Al(OH)3+3H+ |
| C、足量氢氧化钠溶液与碳酸氢钠溶液混合:OH-+HCO3-═H2O+CO32- |
| D、表示氢气燃烧热的化学方程式:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-不能大量共存(常温下) | ||
B、
| ||
| C、已知:25℃时,Mg(OH)2的kSP=5.61×10-12,MgF2的kSP=7.42×10-11、25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2可以转化为MgF2 | ||
| D、在6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑反应中,XeF4按已知方式水解,每生成4mol Xe,转移16mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将0.2mol/L某强碱弱酸盐NaA溶液与0.1mol/L盐酸等体积混合,混合后溶液显碱性,则混合溶液中 c(HA)>c(Cl-)>c(A-)>c(OH-) |
| B、相同条件下,向氨水、氢氧化钠溶液中分别加入适量的氯化铵晶体后,两溶液的pH:前者减小,后者增大 |
| C、室温条件下,将pH=3盐酸VaL与pH=11氢氧化钠溶液VbL混合,混合后溶液pH=4,假设混合后忽略体积变化,则Va:Vb=10:9 |
| D、0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用硫酸钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔知滤纸上写“嫦娥奔月”,会出现红色字迹,据此下列叙述正确的是( )
如图某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用硫酸钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔知滤纸上写“嫦娥奔月”,会出现红色字迹,据此下列叙述正确的是( )| A、铅笔端作阴极,铂片端发生还原反应 |
| B、铅笔端有少量钠生成 |
| C、硫酸钠溶液不可用硝酸钾溶液代替 |
| D、铂片端发生的电极反应为:40H--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| n(Fe3+) | ||
n(C2
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com