
| A. | 在反应①中,生成3mol汞,转移3mol电子 | |
| B. | 在反应②中,硫化汞既是氧化产物,又是还原产物 | |
| C. | 在反应③中,产生11.2L氧气,转移2mol电子 | |
| D. | 由反应③知,汞在空气中加强热会生成氧化汞 |
分析 在硝酸汞[Hg(NO3)2]溶液中插入一块已清洗掉氧化摸的铝片,片刻后,观察到铝片表面有大量“白毛”(生成了汞)反应的方程式为:2Al+3Hg(NO3)2=2Al(NO3)3+3Hg;
②向剧毒的水银表面撒一层硫粉,汞转化成硫化汞(HgS),方程式:Hg+S═HgS;
工业上,用热分解法冶炼汞:加热氧化汞得到汞蒸气,方程式:2HgO$\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑,依据方程式结合氧化还原反应基本概念解答.
解答 解:A.依据方程式:2Al+3Hg(NO3)2=2Al(NO3)3+3Hg,可知生成3mol汞转移6mol电子,故A错误;
B.依据方程式:Hg+S═HgS,可知汞化合价升高,硫化合价降低,所以HgS既是氧化剂又是还原剂,故B正确;
C.2HgO$\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑,题干中为指明气体状态,气体摩尔体积未知,无法计算转移电子的物质的量,故C错误;
D.由2HgO$\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑,可知氧化汞不稳定,受热易分解,汞在空气中加热不能生成氧化汞,故D错误;
故选:B.
点评 本题考查了氧化还原反应,明确物质的性质及发生反应的方程式、熟悉氧化还原反应基本概念是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
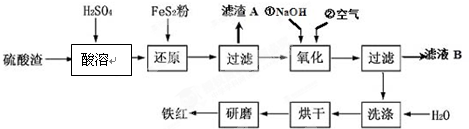
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
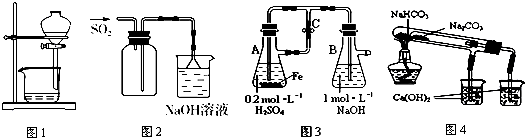
| A. | 图1用于放出碘的苯溶液 | |
| B. | 图2用于实验室收集SO2 | |
| C. | 图3用于实验室制备Fe(OH)2 | |
| D. | 图4用于比较NaHCO3和Na2CO3热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂 1mol N-N键吸收193kJ热量,断裂 1mol N≡N键吸收941kJ热量,则下列说法不正确的是( )| A. | N4与N2互为同素异形体 | |
| B. | 1 mol N4气体转化为N2时要放出724 kJ能量 | |
| C. | N4变成N2是化学变化 | |
| D. | N4不可能是分子晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com