
【题目】甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇. 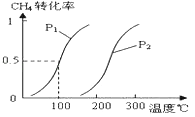
(1)将1.0mol CH4和2.0mol H2O(g)通入容积为10L的反应室,在一定条件下发生反应Ⅰ:CH4(g)+H2O(g)CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图:
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为 .
②在其它条件不变的情况下升高温度,化学平衡常数将(填“增大”“减小”或“不变”).
③图中的P1P2(填“<”、“>”或“=”),100℃时平衡常数为 .
④保持反应体系为100℃,5min后再向容器中冲入H2O,H2各0.5mol,化学平衡将向移动(填“向左”“向右”或“不”).
(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发发生反应Ⅱ:
CO(g)+2H2(g)CH3OH(g)
①该反应的△H0,△S0(填“<”、“>”或“=”).
②若容器容积不变,下列措施可以提高CO转化率的是 .
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大
D.再充入1mol CO和3mol H2 .
【答案】
(1)0.030mol?L﹣1?min﹣1;增大;<;2.25×10﹣2;向左
(2)<;<;BD
【解析】解:第(1)问:①由100℃平衡CH4的转化率为0.5可知,消耗CH4为1mol×0.5=0.5mol,平衡时甲烷的浓度变化量为: ![]() =5×10﹣2mol/L,根据甲烷与氢气的计量数关系,则:v(H2)=3v(CH4)=3×
=5×10﹣2mol/L,根据甲烷与氢气的计量数关系,则:v(H2)=3v(CH4)=3× ![]() =0.030molL﹣1min﹣1 ,
=0.030molL﹣1min﹣1 ,
所以答案是:0.030molL﹣1min﹣1;②通过图表可知当温度相同时,p2→p1时,甲烷的转化率提高,平衡向正向移动,正向为气体系数增大的反应,根据减小压强平衡向系数增大的方向移动可得出p1<p2;当压强为p1时,升高温度,甲烷的转化率提高,平衡向正向移动,所以正向为吸热反应,所以升高温度平衡常数变大,所以答案是:增大;③由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,正反应为气体体积增大的反应,增大压强平衡向逆反应方向移动,甲烷的转化率降低,故压强P1<P2 ,
CH4(g) | + | H2O(g) | = | CO(g) | + | 3H2(g) | |
初始浓度: | 0.1 | 0.2 | 0 | 0 | |||
变化浓度: | 0.05 | 0.05 | 0.05 | 0.15 | |||
平衡浓度: | 0.05 | 0.15 | 0.05 | 0.15 |
100℃时平衡常数= ![]() (mol/L)2=2.25×10﹣2 (mol/L)2 ,
(mol/L)2=2.25×10﹣2 (mol/L)2 ,
所以答案是:<;2.25×10﹣2;④保持反应体系为100℃,5min后再向容器中冲入H2O、H2各0.5mol,Qc= ![]() =4×10﹣2>K,所以平衡向左移动,所以答案是:向左;
=4×10﹣2>K,所以平衡向左移动,所以答案是:向左;
第(2)问:①混合气体在催化剂作用下能自发反应生成甲醇,则说明正反应是放热反应,所以△H<0;正反应是气体物质的量减小的反应,气体的物质的量越多,其熵越大,所以△S<0,所以答案是:<;<;②A.该反应为放热反应,升高温度,平衡向吸热方向移动,即向逆反应方向移动,甲醇的产率降低,故A错误;
B.将CH3OH(g)从体系中分离,产物的浓度降低,平衡向正反应移动,甲醇的产率增加,故B正确;
C.充入He,使体系总压强增大,容器容积不变,反应混合物各组分浓度不变,平衡不移动,甲醇的产率不变,故C错误;
D.再充入1mol CO和3mol H2 , 可等效为压强增大,平衡向体积减小的方向移动,即向正反应方向移动,甲醇的产率增加,故D正确,
所以答案是:BD.
【考点精析】通过灵活运用化学平衡状态本质及特征,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图表示不同温度下水溶液中c(H+)与c(OH﹣)的关系,下列判断正确的是( ) 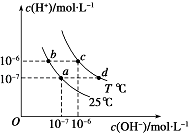
A.两条曲线上任意点均有c(H+)×c (OH﹣)=Kw
B.T<25
C.b点和c点pH均为6,溶液呈酸性
D.只采用升温的方式,可由a点变成d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在一定体积pH=12的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若体积可以加和,则V(Ba(OH)2):V( NaHSO4)为( )
A.1:1
B.1:2
C.1:3
D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)将a mol钠和a mol铝一同投入m g足量水中,请用两个离子方程式表示有关生成H2的变化: . 该溶液的溶质质量分数为 .
(2)在标准状况下,22.4升的密闭容器中充入CO2和CO混合气体,其密度为10/7g/L,加入足量Na2O2充分振荡并不断用点火花点燃至完全反应,则容器中存在molO2 , molNa2CO3 .
(3)取一定量的镁铝合金,用足量盐酸溶解后,再加入过量的NaOH溶液,然后滤出沉淀物,加强热灼烧,最后得到白色粉末,干燥后称量,这些粉末与原合金的质量相等,则合金中铝的质量百分含量为 .
(4)已知2Fe2++Br2=2Fe3++2Br﹣ , 2Br﹣+Cl2=2Cl﹣+Br2 . 往100mLFeBr2溶液中缓慢通入2.24升氯气(标准状况),结果溶液中有三分之一的Br﹣被氧化成Br2 . 求原FeBr2的物质的量浓度 .
(5)部分氧化的Fe﹣Cu合金样品(氧化物为Fe2O3、CuO)共5.76g,经如图处理: 
根据题中条件计算V= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用pH试纸测定某无色溶液的pH时,规范的操作是( )
A. 将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B. 将溶液倒在pH试纸上,跟标准比色卡比较
C. 用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上跟标准比色卡比较
D. 试管内放少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某BaCl2溶液中通入SO2气体,未见沉淀生成;若先通入SO2气体,再通入另一种气体,则可看到沉淀生成;这种气体不可能是( )
A. Cl2B. NH3C. HClD. SO3(气体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数,下列说法中正确的是( )
A.标准状况下,22.4LSO3所含的分子数为NA
B.49g硫酸中所含氧原子的数目为2NA
C.1molNH4+所含质子数为10NA
D.0.5L 0.2 molL﹣1硫酸钠溶液中含有的SO42﹣离子数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3﹣、Cl﹣、SO42﹣离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图: 
回答下列问题:
(1)焰色反应的操作步骤简记为洗、烧、蘸、烧、洗,洗铂丝的试剂是(写名称),若采用焰色反应检测K+时,观察火焰焰色时必须要透过观察.
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除烧杯、玻璃棒、托盘天平、量筒、药匙、胶头滴管,还缺少的仪器为 .
(3)实验③中沉淀量由A→B过程中所发生反应的离子方程式为 .
(4)经分析,该溶液中肯定存在的阳离子有 .
(5)现补充第④组实验:另取100mL废水,加入硝酸酸化,再滴入AgNO3溶液,未见白色沉淀生成,则该废水中一定存在的阴离子除SO42﹣还有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法不正确的是( )
A.测定中和热实验的玻璃仪器只需烧杯、量筒和温度计
B.用25mL碱式滴定管量取13.50mLNa2CO3溶液
C.用10mL量筒量取5.5mL硫酸溶液
D.用广泛pH试纸测得某碱溶液的pH为12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com