
| 元素编号 | 元素性质或原子结构 |
| T | 最高正价与最低负价的代数和为4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正价是+7价 |
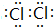 ;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).分析 短周期元素中,T元素的最高正价与最低负价的代数和为4,则T为S元素;X元素原子最外层电子数是次电子数次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为C元素;常温下Y元素单质为双原子分子,其氢化物的水溶液呈碱性,则Y为N元素;Z元素的最高正价是+7价,则Z为Cl,结合对应单质、化合物的性质以及元素周期率解答该题.
解答 解:(1)T为S元素,在元素周期表中的位置为:第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)X的一种同位素可用于测定文物年代,该同位素为,故答案为:614C;
(3)Z单质为Cl2,电子式为 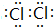 ;Y的氢化物为NH3,其水溶液显碱性的原因为:NH3+H2O?NH3•H2O?NH4++OH-,
;Y的氢化物为NH3,其水溶液显碱性的原因为:NH3+H2O?NH3•H2O?NH4++OH-,
故答案为: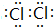 ;NH3+H2O?NH3•H2O?NH4++OH-;
;NH3+H2O?NH3•H2O?NH4++OH-;
(4)同周期自左而右非金属性减弱,Cl元素非金属性比硫的强,
a.物理性质不能说明非金属性强弱,故a错误;
b.氢化物酸性不能比较元素非金属性强弱,故b错误;
c.元素非金属性强弱与获得电子能力强弱有关,与最高正化合价无关,故c错误;
c.非金属性越强,最高价氧化物对应水化物的酸性越强,故d正确;
故答案为:Cl;d.
(5)Z的氢化物为HCl,Y的氢化物为NH3,二者发生化合反应生成NH4Cl,反应的化学方程式为HCl+NH3=NH4Cl,NH4Cl中含有离子键、共价键,
故答案为:HCl+NH3=NH4Cl;离子键、共价键.
点评 本题考查结构性质位置关系综合应用,为高考常见题型,侧重于学生的分析能力的考查,难度不大,推断元素是解题关键,注意掌握金属性、非金属性强弱比较实验事实.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
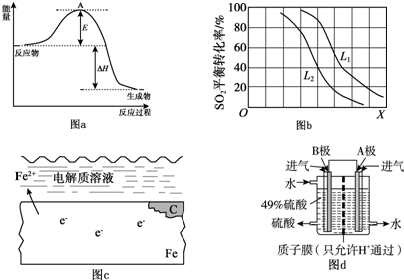
 H2SO32H2SO3+O2
H2SO32H2SO3+O2 2H2SO4.
2H2SO4. 2SO3反应的△H=-198kJ/mol,是放热反应.当压强一定时,温度升高,平衡左移,SO2平衡转化率减小.
2SO3反应的△H=-198kJ/mol,是放热反应.当压强一定时,温度升高,平衡左移,SO2平衡转化率减小.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小.请回答下列问题:
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 方法1 | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
| 方法2 | 用水煤气(主要成分为CO、H2等)将SO2在高温下还原成单质硫 |
| 方法3 | 用Na2SO3溶液吸收SO2转化为NaHSO3,再经电解转化为H2SO4 |
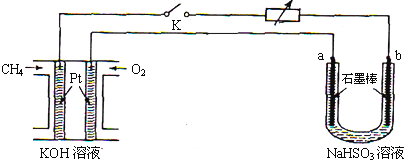
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A. | 醋酸中逐滴加入氢氧化钠溶液 | B. | 硫酸钠中逐滴加入氢氧化钡溶液 | ||
| C. | 硫酸中逐滴加入氢氧化钡溶液 | D. | 盐酸中逐滴加入硝酸银溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com