
| A. | 2NH3(g)═N2(g)+3H2(g)是熵增的反应 | |
| B. | △H、△S分别取“负”时反应一定能自发进行 | |
| C. | 在醋酸溶液中存在两种分子 | |
| D. | 相同温度下,pH值相等的盐酸和醋酸,其浓度是醋酸大于盐酸 |
分析 A.2NH3(g)═N2(g)+3H2(g)中反应前后气体的体积增大;
B.△H-T△S<0的反应,可自发进行;
C.醋酸为弱电解质;
D.HCl为强电解质,而醋酸为弱电解质,醋酸电离不完全.
解答 解:A.2NH3(g)═N2(g)+3H2(g)中反应前后气体的体积增大,则该反应为△S>0的反应,即熵增,故A正确;
B.△H-T△S<0的反应,可自发进行,则△H、△S分别取“负”时,高温下.△H-T△S>0不能自发进行,故B错误;
C.醋酸为弱电解质,在醋酸溶液中存在水分子、醋酸分子,共两种分子,故C正确;
D.HCl为强电解质,而醋酸为弱电解质,醋酸电离不完全,则相同温度下pH=2时,盐酸的浓度为0.01mol/L,醋酸的浓度大于0.01mol/L,即pH值相等的盐酸和醋酸,其浓度是醋酸大于盐酸,故D正确;
故选B.
点评 本题考查反应热与焓变及弱电解质的电离平衡,为高频考点,把握反应进行的方向、pH与浓度的关系、弱电解质电离为解答的关键,侧重分析与应用能力的考查,注意化学反应原理的应用,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
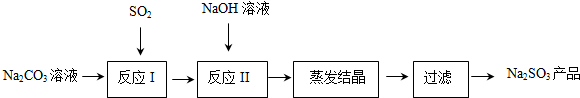
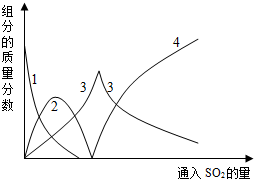
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
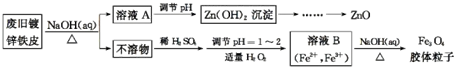
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
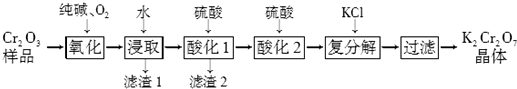
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S的燃烧热为△H=-297.23kJ/mol | |
| B. | S(s)→S(g) 吸收热量 | |
| C. | S(g)+O2 (g)═SO2 (g) 放出的热量小于297.23kJ | |
| D. | 形成1mol SO2化学键所释放总能量大于断裂1molS(s)和1molO2 (g)的化学键所吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
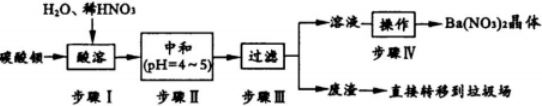
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
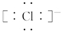 .Al在元素周期表最中的位置是第三周期第IIIA族.
.Al在元素周期表最中的位置是第三周期第IIIA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果5.6LN2含有n个氮分子,则NA一定约为4n | |
| B. | 18g水中所含的电子数是8NA | |
| C. | 在0.5mol/L的氯化钡溶液中含有离子数为1.5NA | |
| D. | 15gCH3+含有8mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com