
| A、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| C、在FeI2溶液中通入少量的氯气:2Fe2++Cl2=2Fe3++2Cl- |
| D、Fe(OH)3与足量的HI溶液反应:Fe(OH)3+3H+=Fe3++3H2O |


科目:高中化学 来源: 题型:
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D、25℃、101 kPa下,Na2O2(s)+2Na(s)═2Na2O(s);△H=-317 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属镁变为镁离子时失去的电子数为2NA |
| B、1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 |
| C、在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA |
| D、CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水玻璃、漂白粉、胆矾均为混合物 |
| B、生成盐和水的反应一定是中和反应 |
| C、NaOH、MgC12、NaC1O、NH4C1均为含共价键的离子化合物 |
| D、煤经过气化或液化两类化学变化过程,可变为清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+和Mg2+ |
| B、O2-和Mg2+ |
| C、F-和Cl- |
| D、Na+和NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 0.5mol?L-1 MgCl2溶液 |
| B、200mL 0.25mol?L-1 AlCl3溶液 |
| C、50mL 1mol?L-1 NaCl溶液 |
| D、25mL 0.5mol?L-1 HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、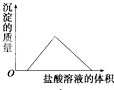 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钙 熟石灰 CaO |
| B、碳酸钙 生石灰 CaCO3 |
| C、氯化钠 食盐 NaCl |
| D、汞 水银 Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 试验次数 | 起 始 温 度T1/℃ | 终止温度T2/℃ | 平均温度差 (T2-T1)/℃ | ||
| H2SO4 溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com