
| (78g/mol��3mol+152g/mol��1mol)��4.145% |
| 32g/mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
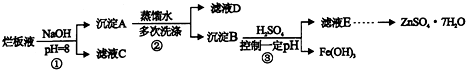
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| A��445.15kJ/mol |
| B��607.3kJ/mol |
| C��890.3kJ/mol |
| D��802.3kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CaCO3��CO2 |
| B��H+��H2 |
| C��Fe2+��Fe3+ |
| D��SO42-��BaSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| A�����Ƕ������ȷ�Ӧ |
| B��a��b��c��Ϊ��ֵ |
| C��a��b |
| D��2b=c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����X+��Y2-�ĺ�����Ӳ�ṹ��ͬ����ԭ��������X��Y |
| B����ˮ��Һ�����ԣ�HCI��H2S�����ƶϳ�Ԫ�صķǽ����ԣ�CI��S |
| C�����ǻ�����ȩ�е���ڶ��ǻ�����ȩ����Ϊ�γ��˷�������� |
| D��H-F��H-O��H-N���ֹ��ۼ��ļ�������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.20mol/L |
| B��0.30mol/L |
| C��0.40mol/L |
| D��0.60mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ᡡ������� ��ȸʯ[Cu2��OH��2CO3] |
| B�����ᡡ���ռ ���̷�[FeSO4?7H2O] |
| C�����ᡡ���Ҵ��� ��̼��� |
| D�����ᡡ����ʯ�ҡ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com