
分别取1 mol葡萄糖进行下列试验:
(1)银镜反应时,生成Ag的物质的量为________ mol,反应后葡萄糖变为________,其结构简式是______________________________.
(2)与乙酸反应生成酯,从理论上讲完全酯化需要________ g乙酸.
(3)若使之完全转化为CO2和H2O,所需氧气的体积在标准状况下为________ L,反应的化学方程式是________________________________.
(1)2 葡萄糖酸铵 CH2OH(CHOH)4COONH4 (2)300
(3)134.4 CH2OH(CHOH)4CHO+6O2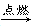 6CO2+6H2O
6CO2+6H2O
【解析】
试题分析:(1)1 mol葡萄糖中含有1 mol醛基,发生银镜反应产生2 mol银,反应后葡萄糖转变为葡萄糖酸铵。
(2)1 mol葡萄糖中含有5 mol羟基,完全酯化需要5 mol乙酸,其质量为300 g。
(3)由反应C6H12O6+6O2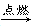 6CO2+6H2O知,1 mol葡萄糖完全转化为CO2、H2O,需6 mol O2,其在标准状况下的体积为134.4 L。
6CO2+6H2O知,1 mol葡萄糖完全转化为CO2、H2O,需6 mol O2,其在标准状况下的体积为134.4 L。
考点:考查葡萄糖的性质和有关计算
点评:该题是中等难度的试题,试题基础性强,注重对学生基础知识的巩固与训练,难度不大。有利于培养学生的规范答题能力,提高学生灵活运用基础知识解决实际问题的能力。


科目:高中化学 来源: 题型:
①称取乳酸0.90 g,升温使其汽化,测其蒸气的密度是H2的45倍。
②将其燃烧并使其产物依次通过碱石灰、无水硫酸铜粉末,碱石灰增重1.42 g,硫酸铜粉末变蓝,继续通入过量石灰水中,有1.00 g白色沉淀生成;在增重的碱石灰中加入盐酸后,产生无色气体,在标准状况下为448 mL。
③另取乳酸0.90 g,跟足量的碳酸钠反应,生成112 mL CO2(标准状况);若跟金属钠反应则生成 224 mL H2(标准状况)。
④乳酸可跟乙酸发生酯化反应,其质量比为3∶2,乳酸可跟乙醇发生酯化反应,其物质的量之比为1∶1,且酯化分别发生在乳酸的链中和链端。
(1)0.90 g乳酸燃烧时,生成CO2__________mol。
(2)乳酸的分子式__________;结构简式__________。
(3)乳酸与乙酸酯化的化学方程式为:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com