
高锰酸钾可用于除去地下水的硫化氢异味的原理是生成的硫和二氧化锰等沉淀物可过滤除去。水体呈弱酸性时,高锰酸钾的还原产物是MnO和MnO2,且MnO和MnO2的物质的量比为3:1。
(1)写出并配平上述化学方程式,标出电子转移方向与数目。
KMnO4 + H2S +H2SO4 →
在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:
KMnO4 + C +H2O →MnO2 + X +K2CO3 (未配平)
(2)X的化学式为__________。
(3) 1mol氧化剂被______(填“氧化”或“还原”)时,生成_____mol氧化产物
(1)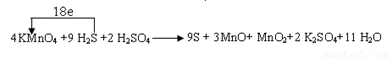 (4分)
(4分)
(2)KHCO3 (2分)
(3)还原 ,0.75 (各1分,共2分)
【解析】
试题分析:(1)由题目信息可知,KMnO4、H2S、H2SO4反应生成S、MnO、MnO2,同时还生成K2SO4、H2O,生成MnO和MnO2的物质的量比为3:1。其中Mn元素的 化合价从+7价降低+2价和+4价,S元素的化合价从-2价升高到0价,设MnO和MnO2的系数分别为为3、1,则根据电子转移守恒可知S的系数为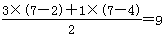 。根据原子守恒可知,KMnO4系数为4,H2S系数为9,K2SO4的系数为2,H2SO4的系数为2,H2O的系数为11,因此配平后方程式为:4KMnO4+9H2S+2H2SO4=9S+3MnO+MnO2+2K2SO4+11H2O,则反应中转移电子数目为9×[0-(-2)]=18,所以标出电子转移方向与数目为
。根据原子守恒可知,KMnO4系数为4,H2S系数为9,K2SO4的系数为2,H2SO4的系数为2,H2O的系数为11,因此配平后方程式为:4KMnO4+9H2S+2H2SO4=9S+3MnO+MnO2+2K2SO4+11H2O,则反应中转移电子数目为9×[0-(-2)]=18,所以标出电子转移方向与数目为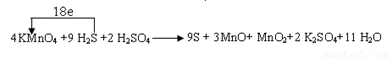 。
。
(2)反应中KMnO4→Mn02,Mn元素化合价由+7价降低为+4价,得到3个电子。C→K2CO3,C元素化合价由0价升高为+4价,失去4个电子。所以化合价升降最小公倍数为12,故KMnO4系数为4,C的系数为3,由C、K的原子数目关系可知K2CO3系数为1,因此X含有+4价的C原子、且C原子与K原子之比为1:1,所以X为KHCO3。
(3)反应中KMn04是氧化剂被还原,发生还原反应。氧化产物为KHCO3、K2CO3,每摩尔KHCO3、K2CO3都含1molC原子,设生成的氧化产物为amol,则根据电子转移守恒可知1mol×(7-4)=amol×(4-0),解得a=0.75。
考点:考查氧化还原反应的有关判断、计算以及配平等


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
(1)若某人不慎使用了劣质香粉,下列物质能用于为他除去黑色斑点的是( )
A.漂白粉 B.高锰酸钾
C.双氧水(H2O2) D.过氧化钠(Na2O2)
(2)说明你选择的理由: 。
(3)去掉黑色斑点的化学原理是(用化学方程式表示): 。
(4)若买到了劣质香粉,你应该怎么办?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com