
| A、O、F、H的原子半径依次减小 |
| B、HI、HBr、HCl、HF的沸点依次降低 |
| C、干冰、钠、冰的熔点依次降低 |
| D、金属Na、Mg、Al的硬度依次降低 |


科目:高中化学 来源: 题型:
| A、2.44 kJ |
| B、4.88 kJ |
| C、44.0 kJ |
| D、88.0 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),NH3和H2的物质的量(n)随时间变化关系如图所示,下列叙述正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),NH3和H2的物质的量(n)随时间变化关系如图所示,下列叙述正确的是( )| A、点e的正反应速率比点d大 |
| B、点c处v(逆)>v(正) |
| C、点d(t1时刻)和点e(t2时刻)处N2物质的量相同 |
| D、图中字母标记的五点中a点对应的NH3的物质的量最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精--易燃品 |
| B、浓硫酸--腐蚀品 |
| C、火药--爆炸品 |
| D、烧碱--易燃品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
| C、CH2=C(CH3)-CH=CH2 |
| D、CH2=CH-CN |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、1:4 |
| C、3:4 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
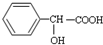 有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )| A、6 种 |
| B、9 种 |
| C、15 种 |
| D、19 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
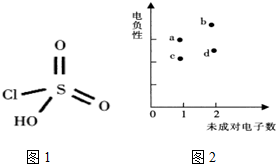 纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1.
纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com