
【题目】观察下列有关实验装置,相关评价错误的是( )

图(1) 图(2) 图(3) 图(4)
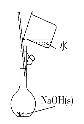
A.图(1)用于配制0.10 mol·L-1 NaOH溶液;评价:正确
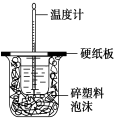
B.图(2)用于测定中和热;评价:错误,装置中缺少了环形玻璃搅拌棒
C.图(3)用于比较Na2CO3、NaHCO3的热稳定性;评价:正确
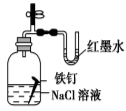
D.图(4)证明铁发生吸氧腐蚀时空气参加反应;评价:正确
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】已知铁的化合物之间有如下转化关系,
![]()
请回答下列有关问题:
(1)Fe与过量稀盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是_________(选填序号);
a.KMnO4 b.HNO3 c.H2O2
(2)硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为-2价)则下列说法正确的是_________(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.Cu2+和S是氧化产物
c.当转移1mol电子时,46g CuFeS2参加反应
d.反应中,CuFeS2既作氧化剂又作还原剂
(3)在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出。
①若滤出的固体中只有铜,则溶液中一定含有的阳离子是 ,一定不含的阳离子是 。
②若滤出的固体中含有铁和铜,则溶液中一定不含的阳离子是 。
(4)高酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,和水发生水解反应生成Fe(OH)3胶体等物质,写出FeO42- 和H2O反应的离子方程式 。高酸钾作为水处理剂发挥的作用是_____________、_____________。 (用简洁的名词描述即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气发生反应的装置。
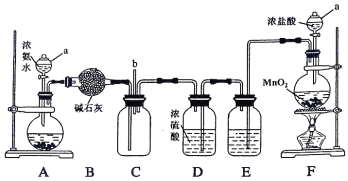
请回答下列问题:
(1)仪器a的名称为 ;装置A的圆底烧瓶中盛放的固体物质可选用___________(填序号)。
a.氯化钠 b.氢氧化钠 c.碳酸钙
(2)装置F的圆底烧瓶中发生反应的离子方程式为 ;装置E的洗气瓶中盛放的试剂为 ,其作用是___________。装置D中浓硫酸的作用是 。
(3)反应过程中,装置C的集气瓶中有大量白烟产生,另一种产物为空气的主要成分之一,该反应的化学方程式为 。
(4)从装置C的b处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有 溶液的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙。
【查阅资料】
Ⅰ、金属Ca的部分性质有:
① 常温或加热条件下Ca都能与氧气反应;;
② Ca常温遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热;
③ Ca+H2![]() CaH2(固体)
CaH2(固体)
Ⅱ、固体CaH2的部分性质有:
①常温:CaH2+2H2O=Ca(OH)2+2H2↑;②CaH2要密封保存。
【进行实验】
该小组同学设计的制取装置如图所示(固定装置略).

回答下列问题:
(1)写出Ca常温遇水发生反应的化学方程式: 。
(2)B、D中所盛试剂相同,该试剂为 (填名称);D中该试剂的作用是 。
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是: 。
【实验反思】
该小组同学通过反思提出问题:上述制得的CaH2是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量为m g的CaH2 样品,按图所示连接仪器(固定装置略)。

步骤2:将Y形管倾斜,使A中的水全部进入B中,样品全部反应后,冷却至室温,读取量筒读数为V mL。
(4)若该实验条件下的气体摩尔体积为Vm L/mol,当V= mL时(用m、Vm表示),表明制得的CaH2样品是纯净的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏伽德罗常数的值。下列说法正确的是
A.该氯原子的相对原子质量为![]()
B.mg该氯原子的物质的量为![]()
C.该氯原子的摩尔质量为aNAg
D.ag该氯原子所含的电子数为17mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用烃A合成高分子化合物N的流程如下:

经测定烃A在标准状况下的密度为1.16 g·L-1;F和G是同系物;核磁共振氢谱显示有机物H中有四种峰,且峰值比为3∶3∶1∶1。
已知:Ⅰ.![]()
![]()

Ⅱ.![]() +R1Cl
+R1Cl![]()
![]() +HCl
+HCl
Ⅲ.R1CHO+R2CH2CHO![]()
![]() +H2O
+H2O
(R1、R2、R3代表烃基或氢原子)
(1) 写出A的结构简式:___________。
(2) H中所含官能团的名称是___________。
(3) H→I、M→N的反应类型分别是______、______。
(4) 写出F和G反应生成H的化学方程式:________________________________。
(5) E和I反应生成M的化学方程式为_________________________________。
(6) 芳香族化合物Q是M的同分异构体,与M具有相同官能团,且水解可以生成 2-丙醇,则Q有____种(不考虑立体异构)。
(7) 请参考以上流程,依照:原料![]() ……→产物模式,设计一个由乙烯合成2-丁烯醛的流程,无机试剂自选。
……→产物模式,设计一个由乙烯合成2-丁烯醛的流程,无机试剂自选。
____________________________________________________________________________________________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的单质.化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①②均为工业上的重要反应。

请回答下列问题:
(1)D的电子式为__ ___。
(2)K的化学式为___ ___。
(3)写出B与C高温反应生成E和F的化学方程式:___ __。
(4)写出D与J的稀溶液反应生成G的离子方程式:__ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4 ![]() 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据________________。
(2)用离子方程式表示除去固体产物中Al2O3 的原理__________________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理________________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:

请回答:
(1)A的组成元素为_____________(用元素符号表示),化学式为__________。
(2)溶液C可溶解铜片,例举该反应的一个实际应用________________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为________。写出该反应的离子方程式______________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是生活生产中常见的物质,表中列出了它们的(主要)成分。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
名称 | 酒精 | 醋酸 | 火碱 | 食盐 | 铜导线 | 亚硫酸酐 | 苏打 |
主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | SO2 | Na2CO3 |
(1)请你对表中①~⑦的主要成分进行分类(填编号):属于电解质的是_________,属于非电解质的是______________。
(2)过量②的水溶液与⑦反应的离子方程式______________________。
(3)某同学用⑤和浓硫酸共热来制备⑥,化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
①请用双线桥标出电子转移的方向和数目;
②被氧化与未被氧化的H2SO4的物质的量之比为___________,当电子转移0.1mol时,消耗还原剂的质量为_______________。
(4)如图1表示某同学配制480mL 0.5mol/L 的NaOH溶液的部分操作示意图,其中有错误的是___________,这样操作所配制的溶液比要求的浓度要___________ (填“偏高”、“偏低”、“不影响”)。配制应称取___________gNaOH。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com