
科目:高中化学 来源: 题型:
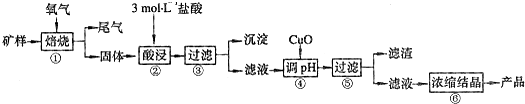
| ||
| ||
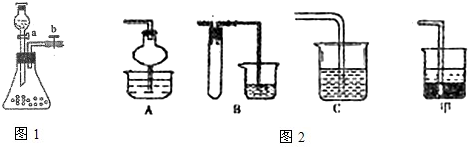
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
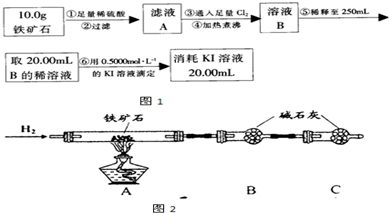
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
| ||
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
某铁的氧化物用1.4 mol?L-1盐酸50Ml恰好溶解,所得溶液还能和56mL(标准状况下)Cl2反应,那么该氧化物的化学式为
A.Fe2O3 B.Fe3O4
C.Fe4O5 D.Fe5O7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com