
分析 元素的金属性越强,其单质与水或酸反应越剧烈,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强、其单质与氢气化合越容易,其氢化物的稳定性越强,据此分析解答.
解答 解:元素的金属性越强,其单质的还原性越强,所以其单质与水或酸反应越剧烈,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强,其单质的氧化性越强,所以其单质与氢气化合越容易,其简单阴离子的还原性越弱,所以其氢化物的稳定性越强,
故答案为:反应;碱性;酸性;难易程度;稳定性.
点评 本题考查元素金属性和非金属性元素周期律,为高频考点,明确金属性、非金属性强弱判断方法是解本题关键,不能根据得失电子多少判断金属性、非金属性强弱,要根据其得失电子难易程度判断,题目难度不大.


科目:高中化学 来源: 题型:解答题
 (1)机动车尾气和燃烧产生的烟气含氮的氧化物,可以用CH4催化还原NOx消除氮氧化物的污染.
(1)机动车尾气和燃烧产生的烟气含氮的氧化物,可以用CH4催化还原NOx消除氮氧化物的污染.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、K+、SO42- | B. | CO32-、NO3-、HCO3-、Na+ | ||
| C. | Na+、ClO-、AlO2-、NO3- | D. | Cu2+、K+、Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .F的原子结构示意图为
.F的原子结构示意图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④ | B. | ⑤ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 A>B>C | B. | 气态氢化物的稳定性HA>H2B>H3C | ||
| C. | 阴离子还原性C3->B2->A- | D. | 非金属性A>B>C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

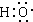 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
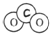
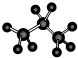

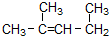 名称为1,3-二甲基-2-丁烯
名称为1,3-二甲基-2-丁烯| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:选择题
下列关于实验基本操作的叙述,不正确的是
A. 用蒸发皿进行加热蒸发时,不需要垫加石棉网即可直接进行加热
B. 蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体发生局部过热而暴沸
C. 蒸馏时,冷凝水应从冷凝管上口进,下口出
D. 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2O含有2mol氧元素 | |
| B. | 1.8gNH4+中含有的质子数为NA | |
| C. | 3.4g氨气中含有0.6NA个N-H键 | |
| D. | PCl3和HCl分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com