
 ��A��B��C��D�����л��A��B��C�������������ʣ�D�����������A�Ǻ����������л�����ӽṹΪ�������壻B�����ģ��Ϊ
��A��B��C��D�����л��A��B��C�������������ʣ�D�����������A�Ǻ����������л�����ӽṹΪ�������壻B�����ģ��Ϊ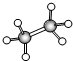 ��C�ı���ģ��Ϊ
��C�ı���ģ��Ϊ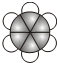 ��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ��
��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ�� CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O�� ���� A�Ǻ����������л�����ӽṹΪ�������壬ӦΪCH4��B�����ģ��Ϊ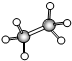 ��ӦΪCH3CH3��C�ı���ģ��Ϊ
��ӦΪCH3CH3��C�ı���ģ��Ϊ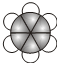 ��Ϊ
��Ϊ ��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ��˵�������ǻ���ӦΪCH3CH2OH��
��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ��˵�������ǻ���ӦΪCH3CH2OH��
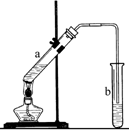
�Ҵ���������Ũ���������·���������Ӧ���������������������������ڱ���̼������Һ�����ᡢ�Ҵ����ܣ�Ӧ��ֹ�������Դ˽����⣮
��� �⣺A�Ǻ����������л�����ӽṹΪ�������壬ӦΪCH4��B�����ģ��Ϊ ��ӦΪCH3CH3��C�ı���ģ��Ϊ
��ӦΪCH3CH3��C�ı���ģ��Ϊ ��Ϊ
��Ϊ ��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ��˵�������ǻ���ӦΪCH3CH2OH��
��D����Է�������Ϊ46������Na��Ӧ����������NaOH��Һ��Ӧ��˵�������ǻ���ӦΪCH3CH2OH��
��1��DΪ�Ҵ����ṹ��ʽΪCH3CH2OH���ʴ�Ϊ��CH3CH2OH��
��2���ж�����������ζ���Ҳ�����ˮ���ܶȱ�ˮС���DZ����ܶȱ�ˮС��������ˮ���������ڱ��У��ϲ�Ϊ��ɫ���²�Ϊ��ɫ��
�ʴ�Ϊ������Һ���Ϊ���㣻�ϲ�Ϊ��ɫ���²�Ϊ��ɫ��
��3������������ṹ���ƣ���Ϊͬϵ������������顢�����顢������3��ͬ���칹�壬�ʴ�Ϊ��ͬϵ� 3��
��4�����Ҵ���������Ũ���������·���������Ӧ���������������������������ڱ���̼������Һ�����ᡢ�Ҵ����ܣ���������̼���Ʒ�Ӧ�����ñ���̼������Һ���ӣ�
�ʴ�Ϊ������Na2CO3��Һ�� ��ȥ���ᣬ�ܽ��Ҵ�����������������ˮ�е��ܽ�ȣ�
�ڴ���������Ũ���������·���������Ӧ����������������Ӧ�ķ���ʽΪCH3COOH+CH3CH2OH CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O��
�ʴ�Ϊ��CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O��
CH3COOCH2CH3+H2O��
���� ���⿼���л����ƶϣ���Ϥ�л���ṹ�������ǽⱾ��ؼ���Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬�ѵ���ͬ���칹��������жϣ���̼���칹���������йصȣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��V��A��Ԫ���γɵ��⻯���зе���ߵ���HI | |
| B�� | ˮ���Ӻ��ȶ�������Ϊˮ���Ӽ����γ���� | |
| C�� | �õ���ʽ��ʾHCl�γɹ��̣�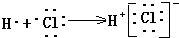 | |
| D�� | ��������Ԫ���γɵļ������У��뾶��С����Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ط��� | X | Y | Z | L | M | Q |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.066 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | +7��-1 | +4��-4 | -2 |
| A�� | ���Ӱ뾶��С��r��X2+����r��Q2-�� | |
| B�� | Y��Q�γɵĻ����ﲻ�ܸ�����������Һ��Ӧ | |
| C�� | MԪ����LԪ���γɵ�һ�ֻ������dz������л��ܼ� | |
| D�� | Z�ĵ��ʿ���������ȼ������ZO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һ | B�� | ʯ����Һ | C�� | Cu��OH��2����Һ | D�� | Na2CO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1L0.5mol/LCH3COOH��Һ�к��е���������Ϊ0.05NA | |
| B�� | �����£�16gO2��O3�Ļ�������к��е���ԭ����ΪNA | |
| C�� | ��״���£�22.4 L NO ��22.4 L O2��Ϻ����������з�������Ϊ1.5 NA | |
| D�� | 1molFeCl3���ˮ��Ӧ���ɽ������NA��Fe��OH��3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ������ʱҪ���մ������ȣ������������ | |
| B�� | �Ȼ����ǵ���ʣ��ɵ����ˮ��Һ��ý����� | |
| C�� | SO2�л�ԭ�ԣ�������Ư��ֽ�� | |
| D�� | ���Ȼ�̼�ܶȱ�ˮ��������ȡ��ˮ�е��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
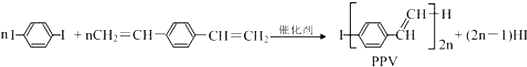
| A�� | PPV�Ǿ۱���Ȳ | |
| B�� | �÷�ӦΪ���۷�Ӧ | |
| C�� | PPV��۱���ϩ����С�ṹ��Ԫ�����ͬ | |
| D�� | 1 mol 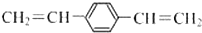 ������2 mol H2������Ӧ ������2 mol H2������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com