
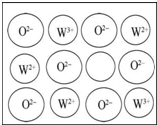
 X��Y��Z��W����Ԫ��ԭ���������������Ҿ�С��36��Z��̬ԭ�����������������ڲ����������3����Y��̬ԭ����ͬ����Ԫ����δ�ɶԵ���������ԭ�ӣ�X�ֱ���Y��ZԪ����Ͼ����γ�10��������W��̬ԭ����10���۵��ӣ��ش��������⣨�������������֪Ԫ�ط������𣩣�
X��Y��Z��W����Ԫ��ԭ���������������Ҿ�С��36��Z��̬ԭ�����������������ڲ����������3����Y��̬ԭ����ͬ����Ԫ����δ�ɶԵ���������ԭ�ӣ�X�ֱ���Y��ZԪ����Ͼ����γ�10��������W��̬ԭ����10���۵��ӣ��ش��������⣨�������������֪Ԫ�ط������𣩣����� X��Y��Z��W����Ԫ��ԭ���������������Ҿ�С��36�� Z��̬ԭ�����������������ڲ����������3����ֻ����2�����Ӳ㣬����������Ϊ6����ZΪOԪ�أ�Yԭ������С��OԪ�أ����̬ԭ����ͬ����Ԫ����δ�ɶԵ���������ԭ�ӣ����ڢ�A�壬��YΪNԪ�أ�X�ֱ���N��OԪ����Ͼ����γ�10����������XΪHԪ�أ�W��̬ԭ����10���۵��ӣ�Ϊ����Ԫ�أ���Χ�����Ų�ʽΪ3d84s2����WΪNi��Ȼ����Ԫ�ػ�����֪ʶ��ԭ�ӽṹ���
��� �⣺X��Y��Z��W����Ԫ��ԭ���������������Ҿ�С��36�� Z��̬ԭ�����������������ڲ����������3����ֻ����2�����Ӳ㣬����������Ϊ6����ZΪOԪ�أ�Yԭ������С��OԪ�أ����̬ԭ����ͬ����Ԫ����δ�ɶԵ���������ԭ�ӣ����ڢ�A�壬��YΪNԪ�أ�X�ֱ���N��OԪ����Ͼ����γ�10����������XΪHԪ�أ�W��̬ԭ����10���۵��ӣ�Ϊ����Ԫ�أ���Χ�����Ų�ʽΪ3d84s2����WΪNi��
��1���� NH3��H2O�pNH2-��OH-�pN3-��O2-�������ƣ���Mg��NH2��2��������þ�������ƣ�һ�������·ֽ�����Mg3N2��NH3����ѧ��Ӧ����ʽΪ��3 Mg��NH2��2�TMg3N2+4NH3����
�ʴ�Ϊ��3Mg��NH2��2�TMg3N2+4NH3����
��2����֪0��ʱH2O���ܶ�Ϊa g/cm3���侧����H2O���ӵĿռ����з�ʽ����ʯ�������ƣ����Ƶ�ԭ���ǣ�ˮ�е�O�ͽ��ʯ�е�C����sp3�ӻ�����ˮ���Ӽ��������з����ԣ�ÿ��ˮ���ӿ������ڵ�4��ˮ�����γ������
������ˮ����λ�ڶ��㡢�����ϣ������ڲ�����4��ˮ���ӣ��ʾ�����ˮ������Ŀ=4+8��$\frac{1}{8}$+6��$\frac{1}{2}$=8��������=$\frac{8��18}{{N}_{A}}$g�������ⳤ=$\root{3}{\frac{\frac{8��18}{{N}_{A}}g}{ag/c{m}^{3}}}$=$\root{3}{\frac{144}{a{N}_{A}}}$cm���ڲ�1��ˮ������1������ˮ�����Լ��ö�������3�����������ˮ���ӹ����������壬������������ⳤ=$\sqrt{2}$��$\root{3}{\frac{144}{a{N}_{A}}}$cm��$\frac{1}{2}$=$\frac{\sqrt{2}}{2}$��$\root{3}{\frac{144}{a{N}_{A}}}$cm����������������ˮ���ӵ��������Ϊy����ˮ���ӷ���֮��ľ���y��������ľ���Ϊb������������Էֳ���ͬ��4�������壨������ˮ������3������ˮ���ӹ��ɣ�����$\frac{1}{3}$��S��y+b��=4��$\frac{1}{3}$����Sb����y=3b�������ⳤ$\frac{\sqrt{2}}{2}$��$\root{3}{\frac{144}{a{N}_{A}}}$Ϊn���������ĵ��������=$\frac{\sqrt{3}}{2}$n cm��$\frac{2}{3}$=$\frac{\sqrt{3}}{3}$n cm���ʣ�$\frac{\sqrt{3}}{3}$n��2+��4b��2=n2�����b=$\frac{\sqrt{6}}{12}$n����y=3b=3��$\frac{\sqrt{6}}{12}$��$\frac{\sqrt{2}}{2}$��$\root{3}{\frac{144}{a{N}_{A}}}$cm=$\frac{\sqrt{3}}{4}$��$\root{3}{\frac{144}{a{N}_{A}}}$cm=��$\root{3}{\frac{144}{a{N}_{A}}}$��1010pm��
������������51kJ/mol��ˮ���Ӽ仹���ڷ��»�����11kJ/mol����1molˮ�к���2mol�����������=���»���+��������Ա�����������ġ����ܡ�=$\frac{1}{2}$����51kJ/mol-11kJ/mol��=20kJ/mol��
�ʴ�Ϊ��ˮ�е�O�ͽ��ʯ�е�C����sp3�ӻ�����ˮ���Ӽ��������з����ԣ�ÿ��ˮ���ӿ������ڵ�4��ˮ�����γ������$\frac{\sqrt{3}}{4}$��$\root{3}{\frac{144}{a{N}_{A}}}$��1010��20��
��3����Ni��28��Ԫ�أ�����ԭ�Ӻ�������Ų����ɿ�֪��Ni2+�Ļ�̬��������Ų�ʽΪ1s22s22p63s23p63d8��ÿ�������˶�״̬������ͬ�����������26���˶�״̬
�ʴ�Ϊ��1s22s22p63s23p63d8��26��
�����ط��ӵĽṹ��ʽΪ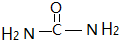 ���������ط�����̼ԭ�ӵ��ӻ���ʽΪsp2�ӻ���ÿ�������к���7���Ҽ�������1mol�����к���7mol�Ҽ������еĦҼ���Ϊ7��6.02��1023��
���������ط�����̼ԭ�ӵ��ӻ���ʽΪsp2�ӻ���ÿ�������к���7���Ҽ�������1mol�����к���7mol�Ҽ������еĦҼ���Ϊ7��6.02��1023��
�ʴ�Ϊ��sp2��7��6.02��1023��
��NO3-��Nԭ�ӹµ��Ӷ�=$\frac{5+1-2��3}{2}$=0���۲���Ӷ���=0+3=3����ռ乹��ƽ���������Σ�
�ʴ�Ϊ��ƽ���������Σ�
����Ϊ��������Ʒ��Ni3+��Ni2+��������֮��Ϊ6��91��������Ԫ�ص�ƽ����Ϊ$\frac{6��3+91��2}{6+91}$=$\frac{200}{97}$���ݻ����ﻯ�ϼ۴�����Ϊ�㣬��$\frac{200}{97}$x=2����x=0.97��
�ʴ�Ϊ��0.97��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰�������㡢��������Ų����ӻ���������ṹ�������֪ʶ�㣬���ضԾ�������Ŀ��飬��Ҫѧ������һ���Ŀռ���������ѧ����������ע�������ѧ��������ṹ���ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

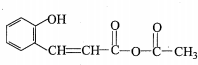 ��G
��G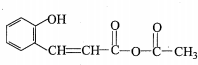

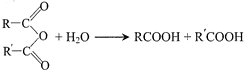
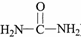 ����ԭ���ϵ���ԭ�ӿ�����A�ϵ���ԭ��������C�����ӳɷ�Ӧ�������۳ɸ߷��ӻ����д��������C��һ���������������Ը߷��ӻ�����Ļ�ѧ����ʽ
����ԭ���ϵ���ԭ�ӿ�����A�ϵ���ԭ��������C�����ӳɷ�Ӧ�������۳ɸ߷��ӻ����д��������C��һ���������������Ը߷��ӻ�����Ļ�ѧ����ʽ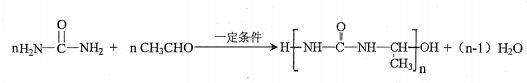
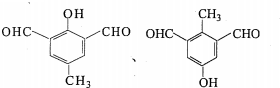 ����һ�֣�
����һ�֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| X | ��ֲ����������ȱ�ٵ�Ԫ�أ��ǵ����ʵ���Ҫ�ɷ� |
| Y | �ؿ��к����ӵ�һλ |
| Z | ����������ԭ�Ӱ뾶��� |
| Q | �����д���ʹ����Ͻ���Ʒ����ҵ�Ͽ��õ����������ķ����Ʊ��䵥�� |
| M | ��ˮ�д���������Ԫ��֮һ������������ϼ��븺�۵Ĵ�����Ϊ6 |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
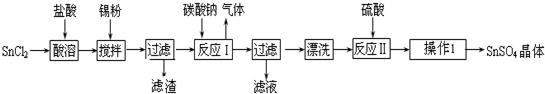
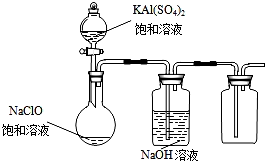 NaClO��KAl��SO4��2������Ҫ�Ļ�����Ʒ������Ӧ������ֽҵ��
NaClO��KAl��SO4��2������Ҫ�Ļ�����Ʒ������Ӧ������ֽҵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
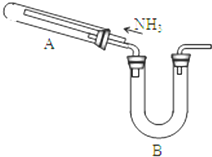 ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ����ͼ��
ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ú�м�������CaO���ɴ�����ȼ�ղ�����SO2���� | |
| B�� | ���Ѿ��еĻ������ڼ��Ի���������ɫ���ʿ����մ�ۼ���ٺ�� | |
| C�� | ʯ���ѽ⡢ú�ĸ��������ƴ��������ʵı��Ժ����������ӵľۼ����ǻ�ѧ�仯 | |
| D�� | ȼ�ϵ������ѵ���SO2�Ļ������ú�NOx�Ĵ�ת�����Ǽ�����������Ĵ�ʩ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com