
把下列四种X溶液,分别加入四个盛有10mL2mol·L-1盐酸的烧杯中,均加水稀释到50mL,此时X和盐酸能缓慢地进行反应。其中反应速率最大的是( )
A、20mL3mol·L-1的X溶液
B、20mL2mol·L-1的X溶液
C、10mL4mol·L-1的X溶液
D、10mL2mol·L-1的X溶液
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:
某同学将铜片加入浓硫酸中,加热后发生反应,探究反应产生的气体产物中是否含有二氧化硫和水蒸气。
(1)写出铜跟浓硫酸在加热条件下反应的化学方程式_______________________________,其中氧化剂是____________。
(2)在上述实验中,铜和浓硫酸应放置在下列_____(填“A”、“B”或“C”)中进行反应。
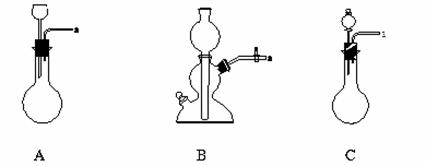
(3)将上述反应装置和下列检验装置连接,检验气体产物,连接顺序为(填连接端点的序号):a→______→______→______。
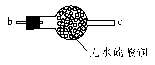

(4)酸雨是指pH小于____________的降水。由二氧化硫形成的酸雨中含一种强酸,该酸是______________,这种酸雨形成过程中的氧化剂是_________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有F e(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
e(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
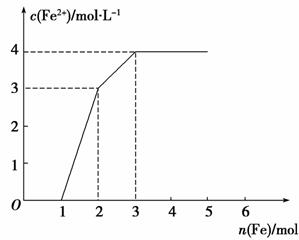
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 mol Cu(OH)2后,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子为( )
A.0.1 mol B.0.2 mol
C.0.3 mol D.0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生氢气的体积(大于25 mL),并检验氯气的氧化性。

(1)A极发生的电极反应式是______ ____________________________,
____________________________,
B极发生的电极反应式是__________________________________________。
电解饱和食盐水的化学方程式____________________________________________。
(2)电源、电流表与A、B两极的正确连接顺序为:
L→( )→( )→( )→( )→M。
(3)设计上述气体实验装置时,各接口的正确连接顺序为:________接________、________接A、B接________、________接________。
(4)在实验中,盛有KI淀粉溶液的容器中发生反应的离子方程式为______________。
(5)已知饱和食盐水50 mL,某时刻测得H2体积为5.6 mL(标准状况)。此时溶液pH约为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
aX(g)+bY(g)cZ(g)+dW(g)在一定容积的密闭容器中反应,5min达到平衡时X减少nmol·L-1,Y减少mol·L-1,Z增加mol·L-1,W增加mol·L-1,则化学方程式中各物质的化学计量数之比a:b:c:d应为( )
A、3:1:2:1
B、1:3:2:2
C、1:3:1:2
D、3:1:2:2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明反应N2+3H22NH3已达到平衡状态的是( )
A、1个N≡N键断裂的同时,有3个N—H形成
B、1个N≡N键断裂的同时,有3个H—H断裂
C、1个N≡N键断裂的同时,有6个N—H断裂
D、3个H—H键断裂的同时,有6个N—H形成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铁及其化合物的说法中正确的是
A.赤铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤
D.Fe3+与KSCN产生红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)H2(g)+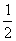 O2(g)====H2O(g) ΔH1= a kJ·mol-1
O2(g)====H2O(g) ΔH1= a kJ·mol-1
(2)2H2(g)+O2(g)====2H2O(g) ΔH2= b kJ·mol-1
(3)H2(g)+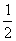 O2(g)====H2O(l) ΔH3= c kJ·mol-1
O2(g)====H2O(l) ΔH3= c kJ·mol-1
(4)2H2(g)+O2(g)====2H2O(l) ΔH4= d kJ·mol-1
下列关系式正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com