
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
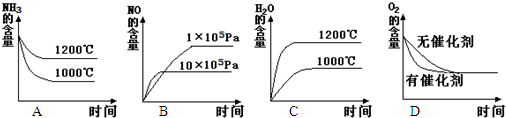
| 时间/浓度/(mol?L-1) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第 2min | 3.2 | 4.5 4.5 |
0.8 | 1.2 |
| 第 4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第 6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
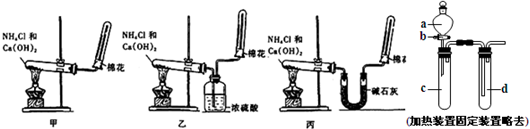
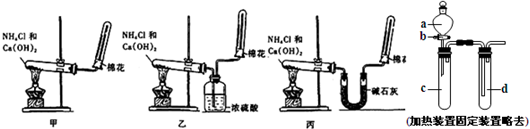
(10分) (1) 氨(NH3)是重要的含氮化合物。1774年该气体由英国普里斯特里制得。为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置。

① 实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) ;
② 写出实验室制取氨气的化学方程式 。
 (2) 一组同学设计出右图所示装置来进行“铁与浓硫酸反应”实验,以探究化学实验的绿色化。
(2) 一组同学设计出右图所示装置来进行“铁与浓硫酸反应”实验,以探究化学实验的绿色化。
① 实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c 。其目的是 。
② 在d中加适量NaOH溶液,向c中放入过量的铁屑和一定量的浓硫酸,塞紧橡皮塞。此时铁屑表面没有气泡生成,说明铁在浓硫酸中发生了_________ ;给试管c加热,当开始有气泡产生时反应的化学方程式是 ,
d中反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com