
| A. | 酸性:H2SO4>H2CO3 | B. | 沸点:CBr4>CCl4 | ||
| C. | 碱性:Al(OH)3>NaOH | D. | 热稳定性:HF>HCl |
分析 A.元素的非金属性越强,则最高价含氧酸的酸性越强;
B.结构相似的分子晶体分子量越大熔点越高;
C.元素的金属越强,对应的最高价氧化物的水化物的碱性越强;
D.元素的非金属性越强,对应的氢化物越稳定.
解答 解:A.元素的非金属性越强,则最高价含氧酸的酸性越强,由于非金属性S大于C,故酸性H2SO4>H2CO3,故A正确;
B.结构相似的分子晶体分子量越大,分子间作用力越强,则熔点越高,故B正确;
C.元素的金属性越强,则对应的碱的碱性越强,由于金属性Na>Al,故碱性NaOH>Al(OH)3,故C错误;
D.元素的非金属性越强,对应的氢化物越稳定,非金属性F>Cl,热稳定性HF>HCl,故D正确.
故选:C.
点评 本题考查了元素周期律的应用,应注意的是元素非金属性和金属性的强弱比较的方法,难度不大,注意基础知识的掌握.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeC13溶液中滴加HI解液:2Fe3++2HI═2Fe2++2H++I2 | |
| B. | 1mol•L-1NaA1O2溶液和4 mol•L-1HCl溶液等体积混合:AlO2++4H+═Al3++2H2O | |
| C. | NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O | |
| D. | Na2S2O3溶液中滴加过量稀H2SO4:3S2O32-+2H+═4S↓+2SO42-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
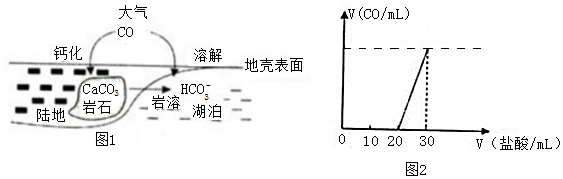
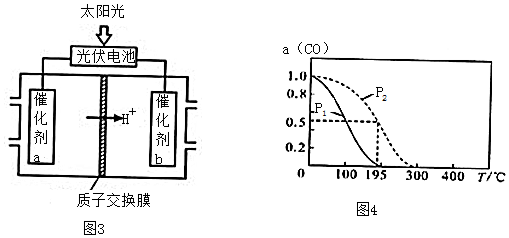
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:1 | B. | 1:5 | C. | 6:1 | D. | 1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜粉加入硝酸中 | B. | 溴化亚铁溶液中通氯气 | ||
| C. | AlCl3溶液中滴入NaOH 溶液 | D. | 铁粉在硫蒸气中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com