
 (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.| 化学键 | H-H | C-O | C-O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1075 | 465 | 413 |
分析 (1)①Fe还原水体中NO3-,根据题意Fe3O4为电解质,则Fe作还原剂,失去电子,作负极;
②NO3-在正极得电子发生还原反应产生NH4+;
(2)反应热=反应物总键能-生成物总键能;根据盖斯定律:反应②-反应①=反应③,反应热也进行相应的计算.
解答 解:(1)①Fe还原水体中NO3-,则Fe作还原剂,失去电子,作负极,
故答案为:铁;
②NO3-在正极得电子发生还原反应产生NH4+,则正极的电极反应式为:NO3-+8e-+10H+=NH4++3H2O,
故答案为:NO3-+8e-+10H+=NH4++3H2O;
(2)反应热=反应物总键能-生成物总键能,故△H1=1076kJ•mol-1+2×436kJ•mol-1-(3×413+343+465)kJ•mol-1=-99kJ•mol-1,
根据盖斯定律:反应②-反应①=反应③,故△H3=△H2-△H1=-58kJ•mol-1-(-99kJ•mol-1)=+41kJ•mol-1,
故答案为:-99;+41.
点评 本题考查化学反应与能量,电化学以及反应热的计算,电极反应式的书写是易错点,注意图中信息的把握,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
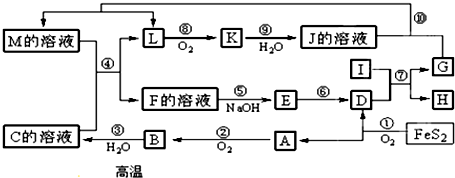
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸遇明火爆炸 | |
| B. | 浓硫酸遇水发热爆炸 | |
| C. | 铁与水反应产生的氢气接触空气遇明火爆炸 | |
| D. | 稀释后的硫酸与铁反应产生的氢气接触空气遇明火爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Al3+ | B. | Al3+ | C. | Fe2+、Al3+ | D. | NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
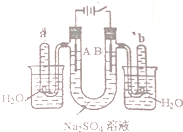 如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )
如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )| A. | 逸出气体的体积,A电极的小于B电极的 | |
| B. | 一电极逸出无味气体,另一电极逸出刺激性气味气体 | |
| C. | A电极附近呈红色,B电极附近呈蓝色 | |
| D. | 电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、Cl-、SO42-、HCO3- | ||
| C. | Na+、CH3COO-、NO3-、K+ | D. | K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气象环境报告中的“PM2.5”是对一种新分子的描述 | |
| B. | 长期使用硫酸铵(NH4)2SO4化肥会使土壤酸化 | |
| C. | “玉兔号”月球车太阳能电池帆板的材料是二氧化硅 | |
| D. | 高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHS 溶于水:NaHS═Na++HS- HS-?H++S2- | |
| B. | (NH4)2SO4溶于水:(NH4)2SO4?2NH4++SO42- | |
| C. | 磷酸溶于水中:H3PO4═3H++PO43- | |
| D. | Al(OH)3的电离:Al(OH)3=Al3++3OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com