
【题目】V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为
A. 56m/V mol·L-1 B. 3m/56V mol·L-1
C. m/56V mol·L-1 D. 3m/112V mol·L-1
科目:高中化学 来源: 题型:
【题目】不洁净玻璃仪器洗涤方法正确的是( )
A.做银镜反应后的试管用氨水洗涤B.做碘升华实验后的烧杯用酒精洗涤
C.盛装CCl4后的试管用盐酸洗涤D.实验室制取O2后的试管用稀盐酸洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量的下列溶液一段时间后,再加入适量的另一种物质(括号内),所得溶液与原来溶液完全一样的是( )
A. CuCl2(CuSO4) B. AgNO3(H2O) C. NaCl(盐酸) D. CuSO4(CuO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)被称为21世纪的新型燃料,25℃,101kPa时呈气态,它清洁、高效、具有优良的环保性能。92g气态二甲醚25℃,101kPa时燃烧放热2910kJ。
(1)写出二甲醚燃烧热的热化学方程式_______________________________________________;当燃烧放出582kJ热量时,转移的电子数为_______________。
(2)已知H2(g)和C(s)的燃烧热分别是285.8kJ/mol、393.5kJ/mo;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为______________________________;
(3)工业上利用H2和CO2合成二甲醚的反应如下:
6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是______________________________(选填字母编号)
A. c(H2)与c(H2O)的比值保持不变
B.单位时间内有2mol H2消耗时有1mol H2O生成
C.容器中气体密度不再改变
D.容器中气体压强不再改变
E.反应产生的热量不再变化
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产量将_______________(填“变大”、“变小”或“不变”,下同),混合气体的平均摩尔质量将_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Na2O2与水反应中,叙述正确的是 ( )
A. O2是还原产物 B. NaOH是氧化产物
C. Na2O2是氧化剂,水是还原剂 D. Na2O2既是氧化剂,又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算后填空
(1)质量都为3g的镁和铝,物质的量之比为;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的盐酸的物质的量之比为 .
(2)在50mL NaNO3和Na2SO4的混合溶液中,c(Na+)=1mol/L,往其中加入50mL BaCl2溶液恰好完全反应,后得到2.33g白色沉淀,则原混合溶液中c(NO3﹣)=mol/L.
(3)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气. 在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂mol,被氧化的物质的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算后填空
(1)质量都为3g的镁和铝,物质的量之比为;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的盐酸的物质的量之比为 .
(2)在50mL NaNO3和Na2SO4的混合溶液中,c(Na+)=1mol/L,往其中加入50mL BaCl2溶液恰好完全反应,后得到2.33g白色沉淀,则原混合溶液中c(NO3﹣)=mol/L.
(3)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气. 在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂mol,被氧化的物质的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当前材料科学的发展方兴未艾。B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_____________________________
(2)BF3分子空间结构为___________;在NH3中N原子的杂化方式为_______。
(3)科学家目前合成了N4分子,结合等电子体相关内容判断该分子中N—N键的键角为__________。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图所示。化合物乙的沸点明显高于化合物甲,主要原因是_________________________________________
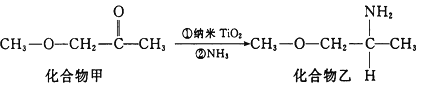
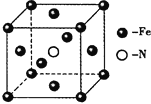
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如右上图所示。若该晶体的密度是ρ g·cm-3,则两个最近的Fe原子间的距离为_____________cm。(阿伏加德罗常数用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙关系正确的是( )
选项 | 甲 | 乙 |
A. | 电解质 | BaSO4、NaHSO4、SO3 |
B. | 弱电解质的电离 | 均分步电离 |
C. | 化学平衡影响因素 | 温度、压强、浓度、催化剂等 |
D. | 化学电源 | 一次电池、二次电池、燃料电池等 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com