
【题目】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)在量取浓盐酸时宜选用下列量筒中的________。
A.5 mL B.10 mL
C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面最低处与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)________。
【答案】 250 C ③①④②
【解析】(1)依据配制溶液的体积选择容量瓶的规格;
(2)依据c=![]() 计算浓盐酸的物质的量浓度,依据稀释前后溶质的物质的量不变计算需要浓盐酸体积,依次选择合适的量筒;
计算浓盐酸的物质的量浓度,依据稀释前后溶质的物质的量不变计算需要浓盐酸体积,依次选择合适的量筒;
(3)依据配制一定物质的量浓度溶液的一般步骤排序;
(1)要配制盐酸220mL,则需要选择250mL的容量瓶;
答案为:250;
(2)浓盐酸的物质的量浓度c=![]() =
=![]() =11.6mol/L,设所需浓盐酸的体积为V,则有V×11.6mol/L=0.25L×1mol/L,得V=0.0216L,即21.6mL,应选择25mL的量筒,故答案为:C;
=11.6mol/L,设所需浓盐酸的体积为V,则有V×11.6mol/L=0.25L×1mol/L,得V=0.0216L,即21.6mL,应选择25mL的量筒,故答案为:C;
(3)配制一定物质的量浓度的溶液的一般操作步骤有计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶,故上述操作中,正确的顺序是③①④②;


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】关于有机物a( )、b(
)、b(![]() )、c(
)、c( )
)
A. a、b、c均能与溴水发生加成反应
B. a、b、c的分子式均为C8H8
C. a的所有原子一定处于同一一平面
D. b的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,草酸溶液中部分微粒的物质的量浓度随NaOH溶液的加入pH 的变化如图所示。其中c (H2C2O4) +c (HC2O4-)+ c (C2O42-)=0.1mol/L,下列说法不正确的是

A. H2C2O4的Ka2数量级为10-5
B. NaHC2O4溶液中,c (Na+)>c(HC2O4-)>c (H+)>c (OH-)
C. 0.1mol/L 的H2C2O4溶液,H2C2O4的电离度为80%
D. pH=7.0的溶液中,c (Na+)=0.1 + c(C2O42-) - c (H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬合金有重要的用途,从其废料中制取铬的流程如下:
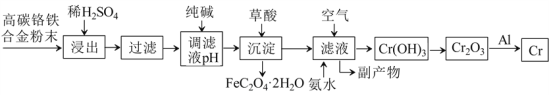
已知: ① Cr+H2SO4=CrSO4+H2↑,
② 流程中铬元素浸出之后至生成Cr(OH)3之间均以自由移动离子状态存在于溶液中。
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有:________________________ (写一条即可) 。
(2)用纯碱调节滤液pH,得到某弱碱沉淀,若纯碱过量,则可能导致的后果是_:_____________。
(3)流程中的“副产物”中,可用作可溶性钡盐中毒解毒剂的物质的化学式是___________;可用作化肥的物质的化学式是_____________。
(4)加入草酸实现沉淀转化反应化学方程式为:_______________________________________。
(5)流程中利用铝热反应冶炼铬的化学方程式为:_____________________________________。
(6)流程中由滤液生成Cr(OH)3的化学方程式为:_____________________________________。
(7)除已知反应①之外,整个流程中涉及的主要氧化还原反应有_____个,分解反应有____个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四物质有如下转化关系(反应条件和部分产物已略去):A![]() B
B![]() C
C![]() D,回答下列问题:
D,回答下列问题:
(1)若A为气态氢化物和D能通过化合反应生成一种盐,则
①简述检验该盐中阳离子的方法:_____________________________________;
②写出实验室制取A的化学方程式:______________________________________;
③写出由A生成B的化学方程式:______________________________________;
④某同学用干燥的圆底烧瓶收集一瓶A气体,用滴入酚酞的水做喷泉实验,能观察到美丽的红色喷泉。用方程式解释喷泉呈红色的原因:____________________。
(2)若A与B反应能生成一种淡黄色固体单质,写出该反应的化学方程式: ________________________________________________________________。
(3)若A是金属单质,C是一种淡黄色固体,写出C生成D的离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中Y形管是一种特殊的仪器,通常与其他仪器组合可以进行某些实验探究。利用下图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。回答下列问题:

(1)广口瓶中间那根玻璃管的作用是:__________________________________________。
(2)实验前需要将BaCl2溶液煮沸,其目的是:_________________________________。
(3)甲中发生反应的化学方程式为:____________________________________________。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体。该反应的化学方程式为:____________________________________________。
(5)实验时,先使甲中产生的足量气体通入BaCl2溶液中,始终无沉淀生成。由此得出的结论是_______。
(6)向上述⑸实验所得溶液中通入乙产生的气体,产生白色沉淀,请写出发生反应的离子方程式:_____。
(7) 请指出该实验的一个不足之处:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 氯气通入冷的氢氧化钠溶液中:Cl2 + 2OH = Cl + ClO + H2O
B. Fe与少量稀硝酸的反应:Fe + 4H+ + NO3 = Fe3+ + NO↑+ 2H2O
C. 碳酸钡溶于醋酸:BaCO3 + 2H+ = Ba2+ + H2O + CO2↑
D. 用石墨电极电解MgCl2 溶液:2Cl + 2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,体积相同的两个容器中,分别充满由![]() 、
、![]() 、
、![]() 三种原子构成的一氧化氮(
三种原子构成的一氧化氮(![]() )和一氧化碳(
)和一氧化碳(![]() )。下列说法正确的是( )
)。下列说法正确的是( )
A. 所含分子数和质量均不相同
B. 含有相同的质子和中子
C. 含有相同的分子数和电子数
D. 含有相同数目的中子、原子和分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同物质的量浓度的下列溶液中,①NH4Cl;②NH3·H2O;③CH3COONH4;④NH4Al(SO4)2。c(NH4+)由大到小的顺序是
A.③①④②B.④①③②C.①④③②D.④③①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com