
| A、1.5L1mol?L-1的NaCl溶液 |
| B、7.5L2mol?L-1NH4Cl溶液 |
| C、15L2mol?L-1的KCl溶液 |
| D、7.5L1mol?L-1的FeCl3溶液 |


科目:高中化学 来源: 题型:
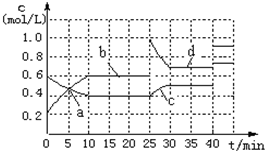
| A、a、b、c、d四个点中处于平衡状态的点是a、b |
| B、反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C、若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D、若40min后出现如图所示变化,则可能是加入了某种催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、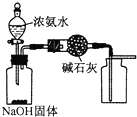 可制取干燥纯净的NH3 |
B、 可以完成“喷泉”实验 |
C、 可测量Cu 与浓硝酸反应产生气体的体积 |
D、 可用于实验室制备Fe (OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从组成元素上可以区别纯净物和混合物 |
| B、往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 |
| C、通过化学变化可以实现16O与18O问的相互转化 |
| D、鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀,属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(8n-m)mol |
| B、(4m-n)mol |
| C、(4n-m)mol |
| D、(7n-m)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用指南针确定航海方向 |
| B、培育新品种,增加农作物产量 |
| C、综合利用石油,合成优良人造纤维 |
| D、设计新程序,开发电脑新功能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始浓度(mol.L-l) | c(NH3) | c(O2) | c(NO) | c(H20) |
| 甲 | 1 | 2 | 0 | 0 |
| 乙 | 4 | 8 | 0 | 0 |
| 丙 | 0.2 | x | y | z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com